13 ФИЗИОЛОГИЯ ЖИДКОСТЕЙ ТЕЛА И ФУНКЦИИ ПОЧКИ
1662 — Л. Беллини (L. Bellini, Италия) открыл канальцы в сосочках
почки (беллиниевы протоки).
1666 — М. Мальпиги (М. Malpighi, Италия) открыл в почках животных сферические
образования (мальпигиево тельце), связанные с кровеносными сосудами.
1782 — А. М. Шумлянский (Россия) установил связь мальпигиева
тельца с канальцами.
1842 — У. Боумен (W. Bowman, Великобритания) описал строение
клубочка почки и его взаимосвязь с канальцами.
1849 — К. Людвиг (К. Ludwig, Германия) высказал мысль о
значении гломерулярной фильтрации и канальцевой реабсорбции в образовании мочи.
1862 — Ф. Генле (F. Henie, Германия) открыл отдел нефрона (петля), названный в
последующем петлей Генле.
1874 — Р. Гейденгайн (R. Heidenhain, Германия) обосновал значение
канальцевой секреции в мочеобразовании.
1883 — И. П. Павлов (Россия) описал
способ наложения фистулы мочевого пузыря у собак для проведения хронических
опытов.
1917 — А. Кешни (A. Cushny, Великобритания) опубликовал первую
монографию о функции почки «Секреция мочи», где сформулировал «современную
теорию образования мочи».
1924 — А. Ричарде (A. Richards, США) осуществил микропункцию
клубочка у лягушки и получил из капсулы безбелковый фильтрат сыворотки крови.
1924 — Э. Маршалл и М. Крейн (Е. Marshall, M. Crane, США) описали секрецию фенолового
красного почкой кролика.
1924 — Л. А. Орбели (СССР) предложил метод раздельного выведения
мочеточников у собак.
1926 — П. Реберг ((Р. Rehberg, Дания) предложил использовать
экзогенный креатинин для измерения клубочковой фильтрации.
1929 — Д. Ван—Слайк (D. Van Slyke, США) предложил понятие «почечный
клиренс» для оценки интенсивности экскреции мочевины.
1943 — Г. Смит (Н. Smith, США) разработал метод клиренсов и
предложил использовать диодраст для исследования почечного кровотока.
1951 — X. Вирц, Б. Харгитей, В. Кун (Н. Wirz, В. Hargitay, W. Kuhn, Швейцария) обосновали и экспериментально
показали роль противоточно—множительной системы в осмотическом концентрировании
мочи.
1958 — А. Г. Гинецинский (СССР) высказал гипотезу о роли гиалуронидазы в
действии антидиуретического гормона в почке.
Более трех миллиардов лет назад в солоноватых
водах возникла жизнь. Длительный путь эволюции привел к развитию клеточной
формы организации, это было связано и с формированием своеобразной
внутриклеточной среды, концентрация ионов в которой отличалась от их содержания
во внешней среде. Такая особенность клеток неизбежно требовала создания
физиологических механизмов,
способствующих регуляции постоянства объема клеток и концентрации в них каждого
из ионов. Сотни миллионов лет спустя на Земле появились многоклеточные
животные, у которых клетки организма были погружены в сформировавшиеся жидкости
внутренней среды.
По мере эволюции живых существ возникли кровеносная система
и специализированные жидкости, такие как цереброспинальная, внутриглазная.
Появление в эволюции системы жидкостей внутренней среды организма представляло
для живых существ преимущество, так как давало им большую независимость от
окружающей внешней среды. Эти жидкости обеспечивают клетки органическими и
неорганическими веществами, в них из клеток поступают конечные продукты обмена
веществ.
В организме животных и человека вода
распределена в нескольких жидкостных фазах. У взрослого человека количество
воды составляет около 60% массы тела, у мужчин по сравнению с женщинами
содержание воды больше из—за меньшего количества жира (табл. 13.1). Из общего
количества воды, принимаемого за 100%, внутри клеток находится 55%, во
внеклеточной жидкости — 45%. Последняя включает воду, содержащуюся в плазме
крови, межклеточной жидкости, в кости и плотной соединительной ткани. Часть
воды входит в состав жидкостей, секретируемых специальными клетками. Это,
например, цереброспинальная, внутриглазная жидкости, а также секреты,
выделяемые железами в просвет желудочно—кишечного тракта.
Общая концентрация растворенных веществ, определяющих осмоляльность
жидкости (или ее осмотическое давление), практически одинакова в клетках и
окружающей их внеклеточной жидкости.
Однако эти жидкости принципиально отличаются друг от друга
по концентрации отдельных ионов, что имеет исключительно большое значение для
нормального осуществления практически всех функций живых клеток. Во
внеклеточных жидкостях в наибольшей концентрации содержатся ионы натрия, хлора,
кальция, внутри клеток — калия, магния, фосфатов и органических кислот (табл.
13.2).
В плазме крови часть ионов связана с белками, часть —
свободна. Белки остаются в плазме крови. Во внеклеточной жидкости содержание
белка мало, поэтому в ней ниже концентрация ионов, связанных с белками (Са2+,
Mg2+).
Таблица
13.1
Объем жидкостных фаз тела у взрослого человека, % от массы
тела
|
Жидкостные фазы тела |
Мужчины |
Женщины |
|
Общее содержание воды |
60,6 |
50,2 |
|
Внутриклеточная жидкость |
33,0 |
27,5 |
|
Внеклеточная жидкость |
27,0 |
22,5 |
|
• межклеточная жидкость |
12,0 |
10,0 |
|
• плазма крови |
4,5 |
3,7 |
|
• внеклеточная жидкость плотной соединительной ткани |
4,5 |
3,7 |
|
• внеклеточная жидкость кости |
4,5 |
3,7 |
|
Жидкость желудочно—кишечного тракта, цереброспинальная, внутриглазная |
1,5 |
1,3 |
Таблица
13.2
Концентрация
электролитов и неэлектролитов в жидкостных фазах у человека, ммоль/л
|
Исследуемое
вещество |
Плазма
крови |
Межклеточная
жидкость |
Внутриклеточная
жидкость в скелетной мышце |
|
Катионы |
|||
|
Натрий |
142 |
145 |
10 |
|
Калий |
4,0 |
4,1 |
159 |
|
Кальций |
2,5 |
1,8 |
1,5 |
|
Магний |
0,9 |
0,7 |
13 |
|
Анионы |
|||
|
Хлор |
104 |
117 |
3,0 |
|
Бикарбонат |
26 |
28 |
7,0 |
|
Анионные
группы белков, фосфаты, органические кислоты |
21 |
8,0 |
154 |
|
Неэлектролиты |
|||
|
Глюкоза |
4,7 |
5,0 |
|
|
Мочевина |
5,0 |
5,5 |
6,0 |
Таблица
13.3
Осмоляльность и концентрация ионов в воде некоторых водоемов и жидкостях внутренней среды животных и человека
|
Объект
исследования |
Осмоляльность,
мосм/кг Н2О |
Концентрация
ионов, ммоль/л |
||||
|
Na+ |
К+ |
Са2+ |
Mg2+ |
S042— |
||
|
Мировой
океан |
1000 |
470 |
10 |
10,2 |
52 |
27 |
|
оз.Байкал |
— |
0,18 |
0,02 |
0,4 |
0,12 |
— |
|
р. Волга |
— |
1 |
0,08 |
0,7 |
0.4 |
— |
|
Гемолимфа |
||||||
|
мидия |
1000 |
472 |
13,5 |
10,3 |
54 |
28 |
|
Кровь |
||||||
|
дождевой
червь |
— |
86 |
5,5 |
8,3 |
— |
— |
|
Сыворотка
крови |
||||||
|
миксина |
1002 |
554 |
6,8 |
8,8 |
23,4 |
1,7 |
|
минога |
248 |
120 |
3,2 |
2,0 |
2,1 |
2,7 |
|
акула |
1075 |
269 |
4,3 |
3,2 |
1,1 |
1 |
|
керчак |
330 |
166 |
2,5 |
3,1 |
0,9 |
— |
|
лягушка |
222 |
108 |
2,6 |
2,3 |
1,2 |
— |
|
голубь |
301 |
147 |
4,0 |
2,6 |
0,7 |
— |
|
человек |
290 |
141 |
4,0 |
2,5 |
0,9 |
0,5 |
Внутри клеток кальций связан, он
находится в эндоплазматической сети, митохондриях. Концентрация свободных ионов
Са2+ в плазме крови составляет около 1,3 ммоль/л, внутри клеток — в
10 000 раз меньше — < 1 х 10—7 моль/л. Кальций играет важнейшую
роль в регуляции функций клетки. Его внутриклеточная концентрация увеличивается
некоторыми гормонами и медиаторами через вторичных посредников.
Общая концентрация всех растворенных в крови веществ у
человека составляет около 290 мосмоль х л—1 (мосм/л), обычно
колебания этого показателя в норме не превышают 1%. Очень точно регулируется и
рН крови на уровне 7,36.
Возникновение жидкостей внутренней среды сопровождалось
развитием физиологических систем регуляции их объема (волюморегуляция),
ионного состава, кислотно—основного равновесия. В океане кровь морских беспозвоночных
имеет такое же осмотическое давление, как и морская вода. Когда происходила
миграция живых существ в пресные воды, а затем и на сушу, потребовалось
появление новой системы — осморегуляции, которая способствовала бы
постоянству осмоляльности крови у живых существ, обитающих в пресных водоемах,
на суше или вновь мигрирующих в море.
Итак, система регуляции водно—солевого обмена должна
обеспечивать постоянство объема, ионного состава, рН и осмоляльности крови и
других жидкостей внутренней среды.
В табл. 13.3 приведены данные о физико—химических
показателях крови животных и жидкостей окружающей их внешней среды. Морские
животные делятся на две группы: одни имеют почти такое же осмотическое давление
внеклеточных жидкостей и крови, как и морская вода, которое меняется
параллельно с изменением осмоляльности среды (пойкилоосмотические
организмы), другие значительно отличаются по осмотическому давлению и
концентрации ионов Na+ от морской воды, но поддерживают постоянной
осмоляльность собственной крови (гомойоосмотические организмы). К первым
относится большинство морских беспозвоночных и миксины, ко вторым —
пресноводные, наземные организмы и морские позвоночные, кроме миксин.
У большинства многоклеточных животных
сформированы органы выделения, которые удаляют избыток жидкости, отдельных
ионов, конечные продукты обмена веществ. У пойкилоосмотических животных органы
выделения не способны к осморегуляции, поэтому при изменении осмоляльности
внешней среды осмотическое давление крови и внеклеточных жидкостей меняется.
Вследствие того что плазматическая мембрана клеток проницаема для воды,
происходит изменение объема клеток.
Изменение объема клеток неблагоприятно сказывается на их
функции, в связи с чем выработался ряд механизмов противодействия этому
процессу. При повышении осмоляльности морской воды, а вслед за тем гемолимфы,
клетки сморщиваются, в них начинает повышаться концентрация аминокислот, ионов Na+ и Сl—, из внеклеточной
среды входит вода и восстанавливается исходный объем. Противоположная картина
наблюдается при уменьшении осмоляльности морской воды (например, при
опреснении), в этом случае наступает набухание клеток. В их цитоплазме
уменьшается концентрация аминокислот, натриевый насос удаляет избыток ионов Na+,
благодаря чему исходный объем клетки восстанавливается.
Гомойоосмотические животные могут
иметь меньшее осмотическое давление крови, чем в окружающей водной среде
(например, миноги и костистые рыбы в морской воде), или большее (все пресноводные
организмы и хрящевые рыбы в морской воде). Физиологический механизм гипоосмотической
регуляции удобно рассмотреть на примере морских костистых рыб. В море они
теряют воду через покровы, особенно жаберную поверхность, и обезвоживаются.
Потеря воды происходит по осмотическому градиенту, так как морская вода имеет
большее осмотическое давление, чем кровь и другие жидкости у рыб. Для
возмещения дефицита воды рыбы пьют морскую воду, она всасывается вместе с
солями Na+ и К+ в кровь В жабрах имеются специальные хлоридные
клетки, которые удаляют из крови в морскую воду соли Na+ без воды, чем способствуют
опреснению жидкостей внутренней среды. Часть солей Са2+ и Mg2+ удаляется почками и кишечником.
Подобным образом устроена система
опреснения крови и у других позвоночных, живущих в море. У миног эту функцию
выполняют клетки в жабрах у морских рептилий и морских птиц появились
специальные солевые железы вырабатывающие секрет с концентрацией Na+ в несколько раз более высокой, чем
в плазме крови, и тем самым опресняющие кровь.
Гиперосмотическая регуляция, т. е. способность поддерживать
более высокую концентрацию осмотически активных веществ в крови, чем в
окружающей среде, присуща всем пресноводным, наземным организмам и морским
хрящевым рыбам. У пресноводных животных часть солей сорбируется из внешней
среды специальными клетками в жабрах или покровах тела, часть поступает с
пищей, а избыток воды удаляется почкой. У наземных организмов потребности в
воде и солях полностью обеспечиваются пищей и потреблением воды.
Необычная система осморегуляции
сформировалась у хрящевых рыб и некоторых амфибий. Около 300 млн. лет назад в
девонском периоде предки этих рыб мигрировали из рек в море. В их плазме крови
сохранилась меньшая концентрация Na+, чем в морской воде, а осмотическое
давление крови, напротив, стало выше нее. Это обусловлено накоплением в крови
огромных количеств мочевины и оксида триметиламина. Вследствие высокой
осмоляльности крови создаются условия для движения воды в тело рыб через жабры
и покровы по осмотическому градиенту из морской воды. При поступлении в
организм акул и скатов избыточных количеств солей натрия последние удаляются
солевой железой, проток которой открывается в задний отдел кишечника— эта
железа получила название ректальной.
Однако экскреция натрия и хлора ректальной железой не
обеспечивает осморегуляцию у эласмобранхий (пластиножаберных рыб). Существенное
значение у них имеет физиологическая уремия. Использование мочевины
хрящевыми рыбами и жабами, обитающими в прибрежных морских водах, обусловлено
тем, что она в избытке образуется в организме, нетоксична, осмотически
высокоактивна мембраны большинства клеток свободно проницаемы для нее, что
позволяет мочевине проникать внутрь клеток. Тем самым мочевина не меняет объем
внутриклеточной жидкости, так как ее концентрация одинакова по обеим сторонам
плазматической мембраны. В то же время накопление мочевины в крови и клетках
приводит к повышению в них осмотического давления по отношению к морской воде и
поступлению воды внутрь тела через покровы по осмотическому градиенту.
У беспозвоночных и позвоночных животных органы, участвующие
в поддержании постоянства состава и объема жидкостей внутренней среды весьма
разнообразны (нефридии, почки, солевые железы, жабры, потовые железы и др.).
Существующие данные позволяют представить гипотетическую схему возможной
эволюции клеток выделительных органов.
|
|
|
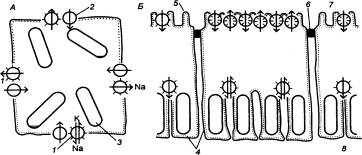
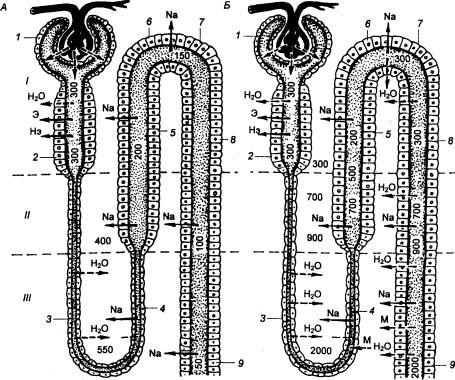
Рис. 13.1 Расположение
ионных каналов и ионных насосов в симметричной (эритроцит) (А) и
асимметричной (нефрон) (Б) клетках 1 — ионный насос, 2
— ионный канал, 3 — митохондрия, 4 — базолатеральная плазматическая мембрана, 5 — люминальная
плазматическая мембрана, 6 — зона межклеточного соединения, 7 — просвет
канальца, 8 — межклеточное пространство. |
В первичной клетке эукариот, из которой в конечном счете
произошли многоклеточные организмы, несомненно поддерживался иной ионный состав
по сравнению с океанической средой. Клетки современных морских беспозвоночных и
позвоночных животных (от простейших до млекопитающих) имеют концентрацию натрия,
калия и других ионов, отличающуюся от окружающей их среды. Согласно современным
представлениям, в плазматической мембране клеток функционируют специфические
для отдельных ионов каналы, по которым ионы могут входить в клетку по
градиенту электрохимического потенциала, и ионные насосы, с помощью
которых удаляется избыток ионов из клетки против электрохимического градиента.
В плазматических мембранах большинства клеток чередуются натриевые каналы и
натриевые насосы (рис. 13.1); их функция и обеспечивает постоянство ионного
состава внутриклеточной жидкости.
Однако на том этапе эволюции, когда произошла
дифференцировка клеток у многоклеточных, возникновение выделительных органов
неизбежно было связано с изменением структуры и функции их клеток, которые
стали осуществлять новую функцию: обеспечивать не только стабильность состава
собственной внутриклеточной жидкости, но и нести ответственность за поддержание
постоянства ионного состава жидкостей организма. Это привело к формированию у
таких клеток способности к направленному транспорту ионов — во внутреннюю среду
организма или из нее во внешнюю среду, иными словами, к сорбции, или секреции
ионов.
Возникла функционально асимметричная клетка, в
которую через одну из мембран непрестанно входят ионы, а с другой стороны клетки
постоянно удаляются. В самой общей форме, с точки зрения молекулярной
организации клетки, это не было связано с возникновением принципиально новых
механизмов, но должно было в результате мутаций и естественного отбора привести
к выживанию особей, у которых с одной стороны клетки в плазматической мембране
будут сосредоточены натриевые каналы, а в мембране другой стороны — натриевые
насосы (рис. 13.1). Таким образом создавалась предпосылка для возникновения
и развития асимметричной клетки, явившейся структурной основой любого
выделительного и осморегулирующего органа.
В целомодуктах (каналах, соединяющих целом с внешней средой)
и нефридиях пресноводных беспозвоночных животных, в почечных канальцах
позвоночных, в слизистой оболочке мочевого пузыря амфибий, коже амфибий, жабрах
пресноводных рыб в апикальной плазматической мембране клеток располагаются
натриевые каналы, а в базолатеральных мембранах — натриевые насосы.
Имеются многочисленные данные, свидетельствующие о том, что
в клетках перечисленных выше органов Na, К—АТФаза сосредоточена в
базолатеральных мембранах клеток.
13.3. ВЫДЕЛИТЕЛЬНЫЕ ОРГАНЫ БЕСПОЗВОНОЧНЫХ ЖИВОТНЫХ РАЗЛИЧНЫХ
ТИПОВ
Осморегуляция, экскреция воды у
пресноводных простейших, а также выделение жидкости у некоторых морских форм
обеспечиваются сократительной вакуолью. У амебы она окружена мембраной,
снаружи от которой располагается зона мелких вакуолей и далее находятся
митохондрии. В пресной воде содержимое сократительной вакуоли у амебы имеет
меньшее осмотическое давление, чем цитоплазмы. Эта вакуоль обеспечивает
экскрецию воды.
У парамеций в цитоплазме содержатся моченосные канальцы,
которые впадают в сократительную вакуоль. Сократительная вакуоль имеется обычно
у пресноводных форм, а у эндопаразитических может отсутствовать. Губки и
кишечнополостные лишены специальных выделительных органов.
Выделение с помощью протонефридия осуществляется у
животных нескольких типов, лишенных целома (плоские черви, немертины, приапулиды
и др.). В ряде случаев они представлены у взрослых животных, обладающих
целомической полостью (некоторые аннелиды), а также у личинок аннелид, у
моллюсков, эхиурид, форонид и др.
Протонефридий представляет собой канадец, проксимальная
часть которого состоит из терминальной клетки с ресничками (пламенная
клетка). Биение ресничек создает отрицательное давление в просвете
нефридиального канальца, благодаря чему в него засасывается жидкость. В
просвете канальца реабсорбируются ионы натрия и вода.
При наличии целомической полости выделительная функция
осуществляется метанефридиями и целомодуктами. Метанефридии
функционируют у аннелид, измененные целомодукты имеются у моллюсков (боянусов
орган), членистоногих (антеннальные железы, максиллярные железы) (рис. 13.2).
Важную роль в экскреции у членистоногих выполняют выросты кишечника из которых
хорошо исследованы мальпигиевы канальцы.
Кольчатые черви обладают полостью тела, в которой находится
целомическая жидкость, и замкнутой системой кровообращения. Нефридиостом
метанефридия открывается в целомическую полость, из которой жидкость поступает
в метанефридий, движется по канальцу (он состоит из нескольких отделов —
узкого, ресничного и широкого) и поступает в мочевой пузырь, из которого
содержимое через нефридиопору выделяется наружу. В канальцах
реабсорбируются соли, в результате образуется гипотоническая моча.
|
|
|
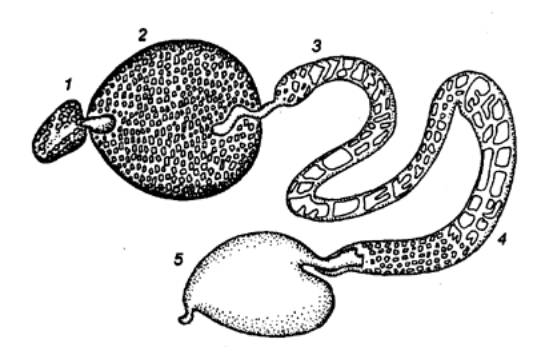
Рис. 13.2
Антенналъная железа речного рака 1 —
целомический мешочек, 2 —
лабиринт, 3 — проксимальный канадец, 4
— дистальный канадец, 5
— мочевой пузырь. |
Перикардиальная полость у моллюсков является остатком целома. В нее через
стенку желудочка сердца фильтруется жидкость, которая по реноперикардиальному
каналу поступает в почечный мешок боянусова органа, движется по
первичному и вторичному мочеточникам и выделяется наружу. Эпителиальные клетки
почечного мешка имеют многочисленные микроворсинки на поверхности, обращенной в
просвет мешка. В боянусовом органе пресноводных моллюсков из фильтрата
всасываются глюкоза, ионы Na+, Cl—. Конечная моча морских моллюсков
изоосмотична гемолимфе, у пресноводных — гипотонична ей.
Процесс образования мочи в антеннальной железе речного рака
имеет черты сходства с почкой позвоночных. Из целомического мешочка жидкость
поступает в просвет железы (см. рис. 13.2). Клетки целомического мешочка
напоминают подоциты клубочка. В процессе мочеобразования жидкость проходит
лабиринт, проксимальный и дистальный канальцы, поступает в мочевой пузырь.
Клетки лабиринта на апикальной мембране имеют многочисленные микроворсинки. Для
клеток дистального канальца характерно наличие многочисленных митохондрий. В
процессе мочеобразования всасываются глюкоза, аминокислоты, вода, ионы Na+,
Сl—. В антеннальной железе
секретируется ряд веществ, в том числе парааминогиппуровая кислота и калий.
13.4. ПОЧКА ПОЗВОНОЧНЫХ ЖИВОТНЫХ
Основным выделительным органом у
позвоночных служит почка. У некоторых животных (морские и проходные
круглоротые, рыбы» рептилии и птицы) ее функция не может обеспечить
осморегуляцию, тогда у них появляются хлоридэкскретирующие клетки в жабрах и
солевые железы.
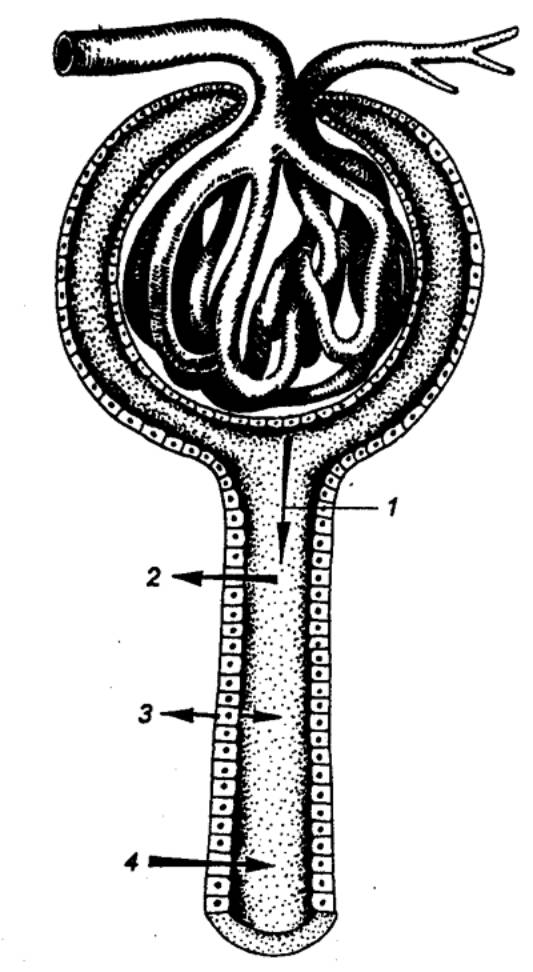
Почка позвоночных построена по единому принципу: структуры,
приспособленные для процесса ультрафильтрации, соединены с системой канальцев,
которые обеспечивают реабсорбцию большинства компонентов профильтровавшейся
жидкости и секрецию ряда веществ в мочу. Нефрон в почке у представителей
всех классов позвоночных обычно начинается с почечного (мальпигиева) тельца. От
полости клубочка отходит шеечный сегмент, в ряде случаев он отсутствует и тогда
париетальный листок, образующий внешнюю часть капсулы почечного клубочка
(боуменовой капсулы), переходит в проксимальный сегмент нефрона (рис. 13.3),
который существует в почках всех позвоночных. Отличительной особенностью его
клеток являются многочисленные микроворсинки, образующие щеточную каемку.
За ним следует промежуточный, или соединительный, отдел, который в почке
млекопитающих образует тонкий отдел петли нефрона (петли Генле). У
большинства животных в почке представлен дистальный сегмент нефрона, в который
могут входить толстый восходящий отдел петли Генле, дистальный извитой канадец
и связующий каналец. Это конечная часть нефрона, которая соединяется с системой
собирательных трубок.
Интенсивность процессов, лежащих в основе образования мочи,
— клубочковой фильтрации, реабсорбции и секреции — не одинакова у
представителей различных классов позвоночных. У круглоротых, рыб, амфибий и
рептилий уровень клубочковой фильтрации составляет 1—4 мл/100 г массы тела за 1
ч» более высокий уровень клубочковой фильтрации наблюдается у птиц, у
млекопитающих он в 10—15 раз выше. Объем фильтруемой жидкости у крыс достигает
50 мл/100 г массы тела за 1 ч.
Такое значительное изменение уровня фильтрации могло
закрепиться в эволюционном процессе только в том случае, если оно сочетается с
эквивалентным увеличением реабсорбции; иначе животное было бы нежизнеспособным.
Действительно, резкое повышение фильтрации у теплокровных сопровождается увеличением
канальцевой реабсорбции. Возросший уровень фильтрации и канальцевой реабсорбции
играет важную роль в более точном поддержании состава всех основных компонентов
жидкой части плазмы крови. Существенное значение имеет повышение кровотока и
фильтрации для работы противоточной системы и осмотического концентрирования
мочи.
|
|
|
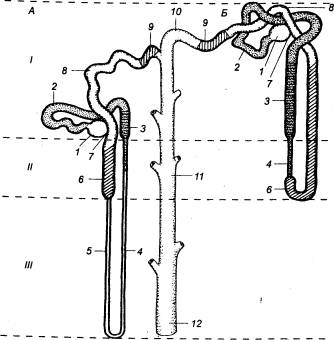
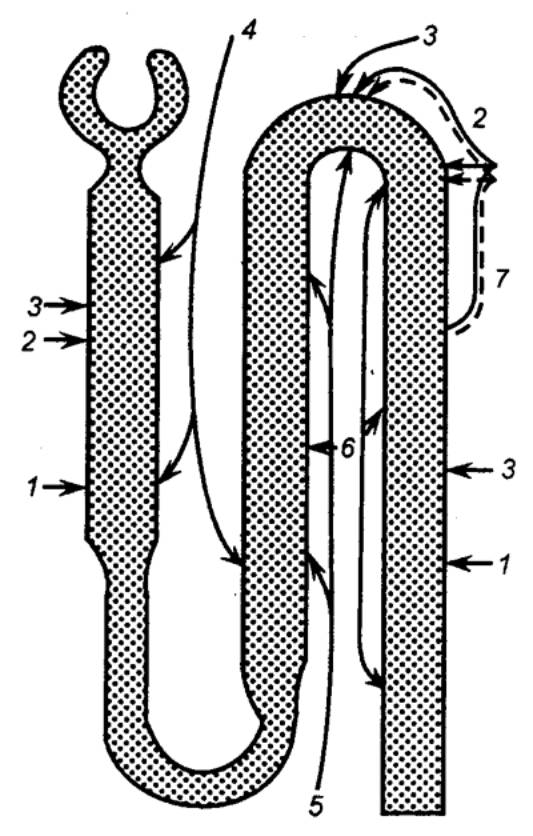
Рис.
13.3 Строение нефрона А — юкстамедуллярный нефрон; JS — суперфициальный нефрон. I — корковое вещество, II — наружная зона мозгового
вещества. III — внутренняя зона мозгового
вещества; 1 — клубочек, 2 — проксимальный извитой канадец 3
— проксимальный прямой канадец 4 — тонкий
канадец (тонкая нисходящая ветвь петли Генле), 5 — тонкий канадец (тонкая
восходящая ветвь петли Генле), 6 —
дистальный канадец (толстая восходящая ветвь петли Генле), 7 — плотное пятно,
8 — дистальный извитой
канадец, 9 — связующий
канадец (в юкстамедуллярном нефроне образует аркаду), 10 — начальные отделы собирательной трубки, 11 — собирательные трубки наружного
мозгового вещества, 12 — собирательные
трубки внутреннего мозгового вещества. |
У человека кровоток в пересчете на 100 г ткани составляет
для почки 430 мл/мин, коронарной системы сердца — 66, головного мозга — 53
мл/мин. Иными словами, почки человека, масса которых составляет около 0 5%
массы тела, в условиях покоя получают около 25% крови, выбрасываемой левым
желудочком, и расходуют до 10% потребляемого организмом кислорода. Учитывая что
на реабсорбцию 22—29 ммоль натрия расходуется 1 ммоль кислорода, и исходя
из допущения, что в процессе эволюции почки энерготраты на перенос натрия не
стали менее эффективными, чем у низших позвоночных, можно понять насколько
возросло расходование энергии почкой, если количество реабсорбированного натрия
увеличилось у высших позвоночных по сравнению с низшими в 20—100 раз. В
процессе естественного отбора эта особенность развития почки удерживалась
именно потому, что она обеспечивала большую стабильность состава внутренней
среды и ее независимость от случайных колебаний во внешней среде.
Так как клубочковая фильтрация осуществляется из
артериальной крови, возрастание объема фильтрации зависело от большего
кровоснабжения почек! У низших позвоночных также возможны ситуации, при которых
необходима усиленная экскреция веществ из крови. Однако обеспечить более
высокий уровень артериального кровоснабжения почки у них было невозможно,
поэтому природа нашла иной выход.
Существенно отметить, что почки
морских костистых рыб, амфибий, рептилии и птиц снабжаются кровью из двух
источников. От аорты к почке подходят артерии, которые дают ветви только
к клубочкам. Эфферентные артериолы клубочков изливают кровь в околоканальцевые
капилляры. В них же поступает кровь и из другого источника — приносящей, ренопортальной
(почечно—воротной) вены. Последняя собирает венозную кровь от задних
конечностей и нескольких вен поясничной области.
Биологическое значение ренопортальной системы состоит в том, что при малом
объеме фильтрации обеспечивается приток крови в околоканальцевые капилляры и
экскреторная функция почки не нарушается, так как эпителий проксимальных
канальцев обладает способностью секретировать из крови в просвет нефрона
некоторые органические вещества, а у морских рыб — и двухвалентные ионы.
13.5. СТРУКТУРА И ФУНКЦИИ ПОЧКИ МЛЕКОПИТАЮЩИХ
Представление о почке только как об
органе выделения никоим образом не соответствует современным данным о широком
круге функций, выполняемых ею в организме. Как уже упоминалось выше, почки
участвуют в регуляции объема жидкостей внутренней среды, концентрации в них
отдельных ионов, суммарной концентрации осмотически активных веществ, рН крови.
Почки обеспечивают экскрецию конечных продуктов азотистого обмена, чужеродных
веществ, избытка органических и неорганических веществ. Важное значение для
организма имеет выработка в почке физиологически активных веществ (ренина,
активной формы витамина D3, эритропоэтина) и ее метаболическая функция, связанная с
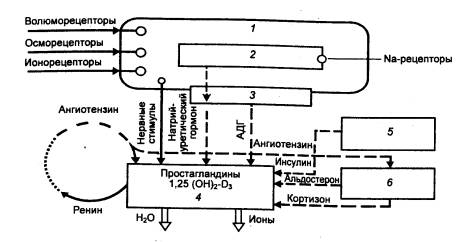
регуляцией обмена углеводов, белков и липидов в организме (рис. 13.4).
Таким образом, почки играют важнейшую роль в поддержании
постоянства основных физико—химических констант крови, регуляции ее объема,
артериального давления, состава ее органических компонентов.
Выполнение почкой этих разнообразных
функций обеспечивают четыре процесса, лежащие в основе деятельности почки: ультрафильтрация
жидкости в почечных клубочках, реабсорбция (обратное всасывание) в
канальцах ценных для организма веществ, секреция (поступление из крови
околоканальцевых капилляров в просвет канальца) ряда веществ, подлежащих
удалению из организма, и синтез новых веществ, которые либо поступают в
кровь, либо удаляются почкой (рис. 13.5).
|
|
|
|
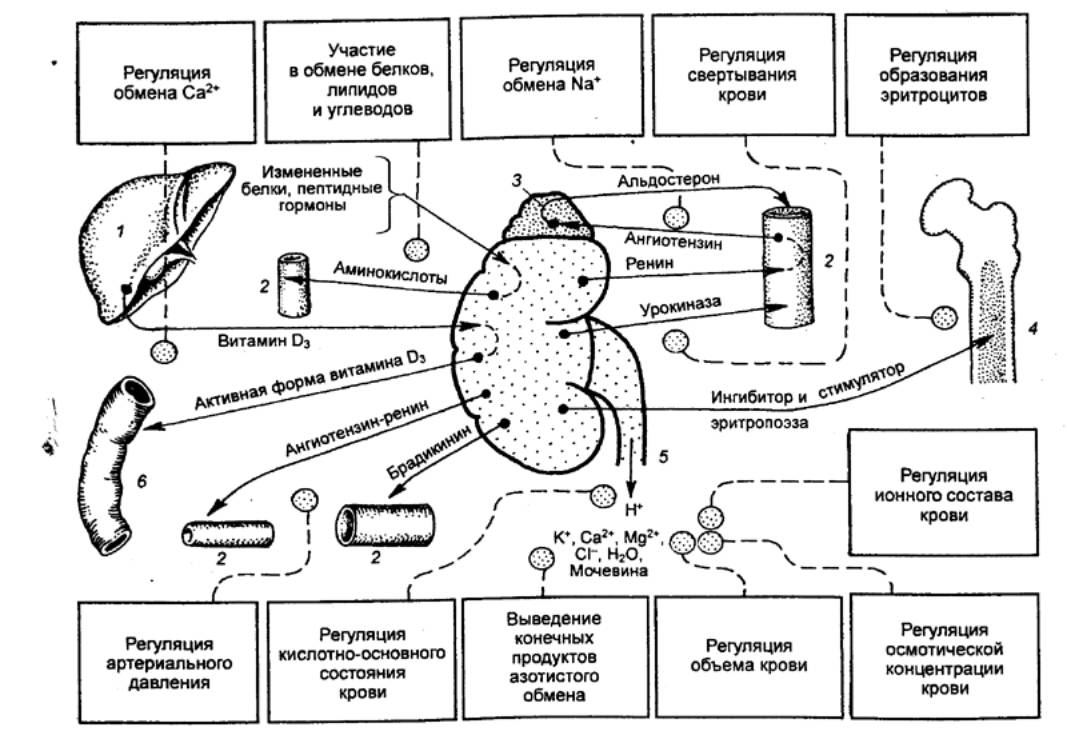
Рис. 13.4 Функции почки у
млекопитающих 1— печень 2 —
артерия, 3 — надпочечник, 4 —
костный мозг, 5 — мочеточник,
6 — кишка. |
|
|
|
||
|
Рис. 13.5 Основные
процессы, обеспечивающие образование мочи 1 — клубочковая фильтрация, 2 — реабсорбция веществ в канальцах, 3 — синтез а секреция
вещества из клетки в просвет нефрона или в сосуд, 4 — секреция вещества клеткой из крови в просвет канальца |
||
|
|
||
|
Рис. 13.6
Строение юкстагломерулярного аппарата 1— юкстагломерулярные клетки, 2 — афферентная артериола,
3— просвет дистального извитого
канальца, 4— эфферентная артериола, 5
— просвет капсулы почечного клубочка (боуменовской капсулы) |
||
Почка млекопитающих структурно состоит из
двух слоев: внешнего, коркового, и лежащего под ним мозгового вещества,
содержащего наружную и внутреннюю части (см. рис. 13.3). Функциональной
единицей почки является нефрон, в почке у человека их насчитывается
около 1 млн. Каждый нефрон начинается с двустенной капсулы почечного клубочка
(Шумлянского—Боумена), внутри которой находится клубочек капилляров. Внешний,
париетальный, листок капсулы Шумлянского—Боумена переходит в проксимальный
сегмент нефрона, состоящий из извитой и прямой частей. Отличительной особенностью
клеток этого сегмента являются многочисленные микроворсинки, образующие
щеточную каемку. В некоторых нефронах имеется очень короткий, в других —
длинный тонкий отдел петли Генле, который соединяется с дистальным сегментом. В
его состав входят толстая восходящая ветвь петли Генле, дистальный извитой
каналец и связующий канадец, который соединен с собирательной трубкой. Функция
каждого из перечисленных отделов нефрона различна.
В почке млекопитающих и человека существует несколько типов
нефронов, отличающихся по расположению клубочков: поверхностные,
интракортикальные (лежащие внутри коркового слоя) и юкстамедуллярные (их
клубочки находятся у границы коры и мозгового вещества). Нефроны разных типов
различаются по длине и структуре петли Генле и участию в процессе осмотического
концентрирования мочи.
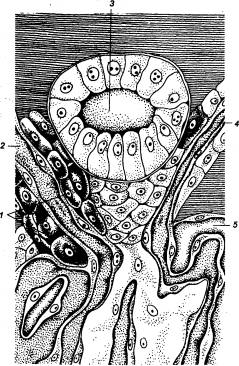
Помимо участия в мочеобразовании
почка, как было показано выше, играет важную роль в качестве инкреторного
органа, в котором образуется ряд физиологически активных веществ. Особое
значение в этом отношении имеет юкстагломерулярный (от лат. juxta — вблизи, glomerulus — клубочек) аппарат, где
синтезируется и секретируется ренин (рис. 13.6). Юкстагломерулярный аппарат образован следующими структурами:
афферентной, приносящей клубочковой артериолой, по которой кровь притекает к
клубочку, эфферентной, выносящей клубочковой артериолой, по которой кровь
оттекает, и клетками плотного пятна дистального извитого канальца. Основное
количество гранул, содержащих ренин, находится в эпителиоидных клетках, которые
замещают мышечный слой в стенке приносящей артериолы. Пространство между
артериолами и дистальным канальцем занято мелкими клетками почечного клубочка.
В 1 мин через сосуды обеих почек у человека проходит около
1200 мл крови, т. е. около 20—25% крови, выбрасываемой сердцем в аорту. Так как
масса почек у человека составляет лишь 0,43% массы тела, очевиден исключительно
высокий уровень органного кровотока. Через сосуды коры почки протекает 91—93%
крови, поступающей в почку, остальное ее количество снабжает мозговое вещество
почки. Кровоток в коре почки в норме составляет 4—5 мл/г ткани. Важной
особенностью почечного кровотока является высокий уровень саморегуляции —
кровоток остается постоянным при изменении артериального давления более чем в
два раза (например, с 90
до 190 мм рт. ст.).
Артерии почки отходят от брюшного отдела аорты, что
обеспечивает высокий уровень артериального давления в приносящих артериолах, по
которым кровь поступает в клубочек, содержащий разветвленную капиллярную сеть.
Кровь от клубочка оттекает по выносящей артериоле, которая вновь распадается на
капилляры вокруг проксимальных и дистальных канальцев; в конечном счете по
венам почки кровь поступает в нижнюю полую вену. Из клубочков юкстамедуллярных
нефронов выносящая артериола доставляет кровь в мозговое вещество, где
образуются прямые артериолы (сосуды), глубоко спускающиеся в него вместе с
петлями Генле и участвующие в осмотическом концентрировании мочи.
13.6.2. Клубочковая фильтрация
Образование мочи в почке начинается
с ультрафильтрации плазмы крови в почечных клубочках. Жидкость проходит
через клубочковый фильтр из просвета кровеносных капилляров в полость капсулы
клубочка. Рассмотрим подробнее структуру этого фильтра и силы, обеспечивающие
процесс ультрафильтрации.
Фильтрующая мембрана. Фильтрующая мембрана состоит из трех слоев:
эндотелия капилляров, базальной
мембраны и внутреннего листка капсулы Шумлянского—Боумена, который образован
эпителиальными клетками — подоцитами.
Клетки эндотелия капилляров имеют очень тонкие
периферические участки, в просвет сосуда выступает лишь область клетки,
где находится ядро. Боковые части клетки пронизаны довольно крупными
отверстиями, обычно затянутыми тонкими диафрагмами. При нормальной скорости
кровотока крупные молекулы белка образуют над этими порами барьерный слой, что
служит препятствием для прохождения через поры не только глобулинов, но и
альбуминов. Таким образом, эндотелий капилляров ограничивает прохождение через
клубочковый фильтр форменных элементов и белков, но свободно пропускает
низкомолекулярные вещества, растворенные в плазме крови.
Следующий барьер гломерулярного
фильтра — базальная мембрана. Ее «поры» ограничивают прохождение молекул
в зависимости от размера, формы и заряда. Так как эта мембрана имеет сетчатую
структуру, образованную тонкими нитями, происходит ограничение прохождения
молекул размером более 3,4 нм. Отрицательно заряженная стенка пор затрудняет
прохождение молекул с одноименным зарядом. Поры не являются круглыми, что также
существенно для ограничения фильтрации альбуминов.
Последним барьером на
пути фильтруемых веществ служат подоциты. Их отростки («ножки»)
прилегают к базальной мембране со стороны капсулы клубочка, между ножками
подоцитов находятся пространства, по которым течет фильтруемая жидкость. Однако
и в этом случае существует заслон на пути фильтруемых веществ — щелевые
мембраны, перегораживающие пространство между ножками подоцитов. Они
ограничивают прохождение альбуминов и других молекул с большой молекулярной
массой. Такой многослойный фильтр в клубочковой мембране обеспечивает
сохранение белков в крови и образование практически безбелковой первичной
мочи.
Ультрафильтрация. Основной силой, обеспечивающей возможность
ультрафильтрации в почечных клубочках, является гидростатическое давление
крови в сосудах. Эффективное фильтрационное давление, от которого
зависит скорость клубочковой фильтрации, определяется разностью между
гидростатическим давлением крови в капиллярах клубочка и противодействующими
ему факторами — онкотическим давлением белков плазмы крови и гидростатическим
давлением жидкости в капсуле клубочка.
Эффективное
фильтрационное давление в клубочках, измеренное у крыс в прямом опыте,
оказалось равным 12 мм рт. ст. (гидростатическое давление крови 47 мм рт. ст.,
онкотическое давление 25 мм рт. ст., внутрикапсулярное давление 10 мм рт. ст.).
По мере того как происходит ультрафильтрация жидкости, онкотическое давление в
крови капилляров растет, потому что белок остается в просвете сосуда и его
концентрация увеличивается. Это приводит к снижению эффективного
фильтрационного давления, которое все более снижается по направлению к тому
участку, где кровь поступает в выносящую артериолу клубочка. в почке у человека
из каждого 1 л плазмы крови образуется 190—200 мл ультрафильтрата. Эта величина
получила название фильтрационной фракции, она представляет собой долю
фильтруемой жидкости из общего объема плазмы крови, притекающей к почечным
клубочкам.
С помощью микроманипулятора и микропипетки из полости
почечного клубочка можно извлечь ультрафильтрат и определить его состав. В нем
такие же, как и в плазме крови, концентрация глюкозы, аминокислот, мочевины,
общее содержание осмотически активных веществ. Между плазмой крови и
ультрафильтратом имеются очень небольшие различия в концентрации одновалентных
ионов, что обусловлено наличием в плазме крови белков, не проходящих через
гломерулярный фильтр и связывающих часть катионов. Это явление носит название равновесия
Доннана.
Особое значение для ультрафильтрации имеет связывание с
белком двухвалентных катионов. С белками связано около 40% ионов Са2+
и 25% ионов Мg2+ от общего их содержания в плазме крови. Остальные
количества этих катионов поступают при ультрафильтрации в капсулу клубочка, где
они представлены в Двух формах: в виде свободных ионов и связанными с
низкомолекулярными анионами. Эти соли свободно проходят через гломерулярный
фильтр. К таким веществам относится, например, цитрат кальция. В плазме крови
человека концентрация кальция составляет 2,5 ммоль/л, при ультрафильтрации в
полость клубочка поступает 1,3 ммоль/л свободных ионов кальция и 0,2 ммоль/л
низкомолекулярных комплексов кальция.
Современные методы позволяют измерить объем жидкости, образующейся
в отдельном почечном клубочке, а также в целой почке. В первом случае для этого
необходимо у животного извлечь микропипеткой жидкость из почечного клубочка, во
втором — получить плазму крови и мочу. В обоих случаях важно точно знать время,
в течение которого образовался ультрафильтрат или моча.
Метод расчета скорости клубочковой фильтрации. Этот метод (при исследовании и
человека, и животных) основан на принципе очищения. Суть его состоит в
следующем. В кровь вводят вещество (например, инулин), свободно
растворяющееся в воде и фильтруемое в почечных клубочках в той же концентрации.
В почечных канальцах его количество не меняется, оно не всасывается в кровь и
не добавляется клетками канальцев из крови в первичную мочу. Определив
количество этого вещества, выделившегося почкой в единицу времени, можно
рассчитать, какой объем крови очистился от этого вещества. Так как этот объем
плазмы крови равен объему жидкости, профильтровавшейся в почечных клубочках,
появляется возможность рассчитать скорость ультрафильтрации жидкости в
гломерулярном аппарате почки, используя метод очищения.
Для измерения клубочковой фильтрации применяют кроме инулина
полиэтиленгликоль—400, маннит. Все эти вещества необходимо вводить в
кровь. Из эндогенных, вырабатываемых в организме веществ, для этой цели
используют креатинин. Общими особенностями веществ пригодных для
измерения клубочковой фильтрации, являются физиологическая инертность,
отсутствие токсичности, свободная растворимость в плазме крови, отсутствие
связывания с белком, свободное проникновение через гломерулярный фильтр в той
же концентрации, что и в плазме крови. Эти вещества не должны реабсорбироваться
и секретироваться в почечных канальцах, а с мочой должны выделяться полностью в
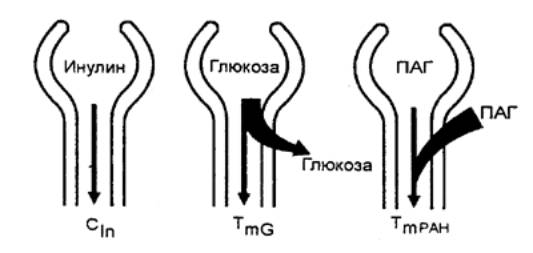
том количестве, которое профильтровалось в почечном клубочке (рис. 13.7).
|
|
|
Рис. 13.7 Определение клубочковой фильтрации по
инулину (Cin), максимальной реабсорбции
глюкозы (ТтG) и максимальной секреции
парааминогиппуровой кислоты — ПАГ (Ттран) Толщина
и направление стрелок указывают на количество выделяемого реабсорбируемого и
секретируемого вещества; объяснение
см. в тексте. |
Эти данные позволяют вывести основную формулу для
определения объема клубочковой фильтрации. Эта величина равна клиренсу (от
англ. clearance — очищение) плазмы крови от инулина (In) и обозначается Cin. Количество
профильтровавшегося в 1 мин инулина равно произведению скорости клубочковой
фильтрации на концентрацию инулина в плазме крови (Pin). Количество инулина, выделяемое с
мочой, равно произведению концентрации инулина в моче на объем выделяемой мочи (V).
Инулин не реабсорбируется и не секретируется, а только фильтруется,
следовательно, CinPin = VUin, откуда
Cin
= UinV / Pin (мл/мин).
Объем выделяемой мочи обычно рассчитывают на поверхность
тела или ее массу. У человека величину объема клубочковой фильтрации относят к
стандартной поверхности тела — человека массой около 70 кг — 1,73 м2.
В норме У мужчин в обеих почках клубочковая фильтрация составляет 125 мл/мин у
женщин эта величина равна 110.
13.6.3. Реабсорбция в канальцах
В почках у человека за 1 сут
образуется около 180 л ультрафильтрата объем выделяемой мочи составляет от 1 до
1,5 л, остальная жидкость реабсорбируется в почечных канальцах. В просвет
почечного канальца поступают все растворенные в плазме крови низкомолекулярные
вещества, а также очень небольшое количество белков. Поэтому основное
назначение системы обеспечивающей обратное всасывание веществ в канальцах,
состоит в том чтобы вернуть в кровь все жизненно важные вещества и в
необходимых количествах а экскретировать конечные продукты обмена веществ,
токсические и чужеродные соединения и физиологически ценные вещества, если они
имеются в избытке. Важное значение имеет фильтрация в клубочках гормонов и
некоторых других физиологически активных веществ, которые в процессе
реабсорбции инактивируются, а их компоненты возвращаются в кровь или удаляются
из организма.
Различные отделы почечных канальцев отличаются по
способности всасывать вещества из просвета нефрона. С помощью анализа жидкости
из отдельных частей нефрона были установлены состав, функциональное значение и
особенности работы всех отделов канальцев почки. В проксимальном сегменте
нефрона из ультрафильтрата в обычных условиях полностью реабсорбируются
глюкоза, аминокислоты, витамины, небольшие количества белка, пептиды, ионы Na+ K+, Са2+,
Mg2+, мочевина, вода и многие другие
вещества. В последующих отделах нефрона органические вещества не
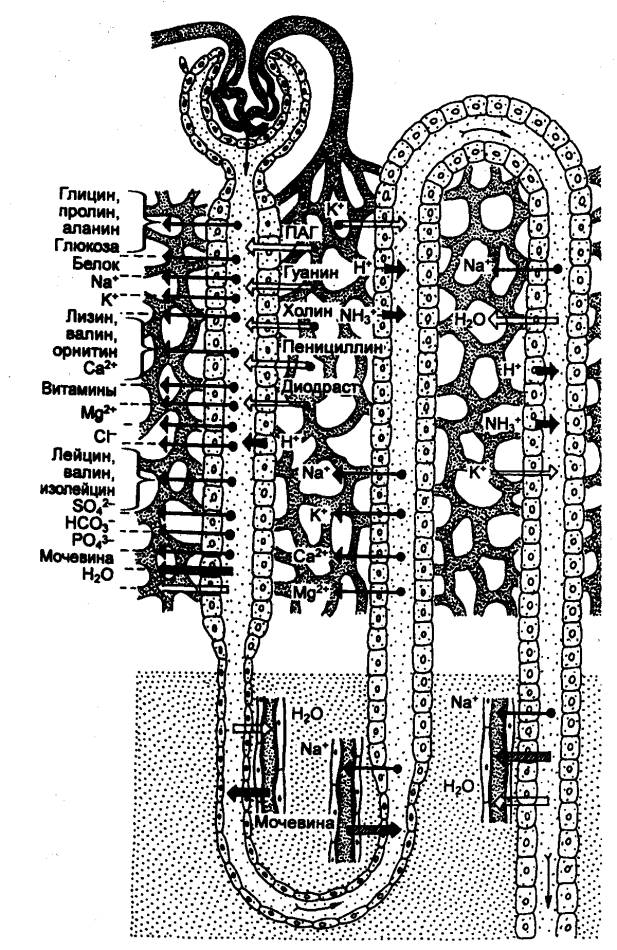
всасываются, в них реабсорбируются только ионы и вода (рис. 13.8).
|
|
|
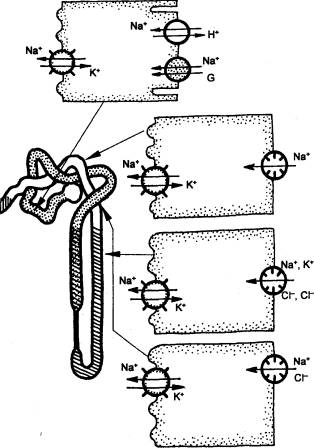
Рис. 13.8 Локализация
реабсорбции и секреции веществ в различных частях почечного канальца |
В проксимальном сегменте нефрона у млекопитающих всасываются
около 60—70% профильтровавшихся ионов Na+ и Сl—, более 90% НСО3—,
перечисленные выше органические и неорганические вещества, доля которых меньше в общей концентрации веществ, растворенных в плазме крови.
Отличительной особенностью
реабсорбции в проксимальном канальце является то, что вслед за всасываемыми
веществами реабсорбируется вода вследствие высокой осмотической проницаемости
стенки этого отдела нефрона. Поэтому жидкость в проксимальном канальце всегда
остается практически изоосмотической плазме крови.
Всасывание отдельных веществ в канальцах обеспечивается
разными способами, их описание поможет понять многообразие молекулярных
механизмов реабсорбции в нефроне.
Клетки эпителия почечных канальцев являются полярными,
асимметричными. Их плазматическая мембрана, обращенная в просвет канальца,
называется люминальной, или апикальной (от лат. apex, apicis — верхушка). Ее свойства во
многих отношениях иные, чем у плазматических мембран боковых частей и основания
клетки, называемых базолатеральными мембранами.
Для понимания физиологических механизмов реабсорбции веществ
существенно, что в люминальной мембране локализованы переносчики и ионные
каналы для многих веществ, обеспечивающие прохождение последних через мембрану
в клетку. В базолатеральных мембранах содержатся Na, К—АТФаза, Са—АТФаза, переносчики
некоторых органических веществ. Это создает условия для всасывания органических
и неорганических веществ из клетки в межклеточную жидкость, в конечном счете —
в сосудистое русло. Наличие в апикальной мембране натриевых каналов, а в
базолатеральных мембранах натриевых насосов обеспечивает возможность
направленного потока ионов Na+ из просвета в клетку канальца и из
клетки с помощью насоса в межклеточное вещество.
Таким образом, клетка функционально является асимметричной,
обеспечивая поток веществ из просвета канальца в кровь. Для такого процесса
имеются структурные и биохимические предпосылки. В базальной части клеток
почечных канальцев сосредоточены митохондрии, в которых при клеточном дыхании
вырабатывается энергия для работы ионных насосов.
Глюкоза. Ежесуточно в канальцы почек у человека поступает 990 ммоль глюкозы, за
сутки в почках реабсорбируется около 989,8 ммоль, т. е. моча оказывается
практически свободной от глюкозы. Следовательно, всасывание глюкозы происходит
против концентрационного градиента, в результате из канальцевой жидкости в
кровь реабсорбируется вся глюкоза при нормальной ее концентрации в крови.
При повышении содержания глюкозы в плазме крови с 5 до 10
ммоль/л глюкоза появляется в моче. Это обусловлено тем, что в люминальной
мембране клеток проксимального канальца находится ограниченное количество
переносчиков глюкозы. Когда они полностью насыщаются глюкозой, достигается ее
максимальная реабсорбция, а избыток начинает экскретироваться с мочой. Величина
максимальной реабсорбции глюкозы имеет важное значение для функциональной
оценки реабсорбционной способности клеток проксимальных канальцев (см. рис.
13.7).
Для определения максимальной величины транспорта глюкозы (ТтG) достигают полного насыщения системы ее канальцевого
транспорта. С этой целью в кровь вводят глюкозу, повышая ее концентрацию в
клубочковом фильтрате до тех пор, пока не будет достигнут порог реабсорбции и глюкоза
не начнет в значительных количествах выделяться с мочой. Величину ТтG рассчитывают по разнице между
количеством профильтровавшейся в клубочках глюкозы (равно произведению объема клубочкового фильтрата Cin на концентрацию глюкозы в плазме
крови РG) и выделившейся с мочой (uG
— концентрация глюкозы в моче, V —
объем выделившейся мочи):
Т тG = СinРG — uGv.
Величина ТтG характеризует полную загрузку
системы транспорта глюкозы У мужчин она равна 2,08 ммоль/мин (375 мг/мин), у
женщин — 1,68 ммоль/мин (303 мг/мин) при расчете на 1,73 м2
поверхности тела.
На примере глюкозы
можно рассмотреть мембранные и клеточные механизмы реабсорбции
моносахаридов и аминокислот в почечных канальцах. В апикальной мембране клеток
проксимального канальца глюкоза соединяется с переносчиком, который должен
одновременно присоединить ион Na+ после чего комплекс приобретает
способность транспортироваться через мембрану. В результате в цитоплазму
клетки поступают и глюкоза, и натрий. Так как мембрана отличается высокой
селективностью и односторонней проницаемостью, она не пропускает глюкозу
обратно из клетки в просвет канальца. Энергетическим источником для переноса
глюкозы через апикальную мембрану служит меньшая концентрация Na+ в
цитоплазме клетки, удаляемого с помощью Na, К—АТФазы, локализованной в
базальной плазматической мембране клетки. Такой процесс получил название вторично—активного
транспорта, когда перенос веществ при их всасывании из просвета канальца в
кровь происходит против концентрационного градиента, но без затраты на
него энергии клетки. Она расходуется на перенос ионов натрия. Первично—активным
называют транспорт в том случае, когда происходит перенос вещества против
электрохимического градиента за счет энергии клеточного метаболизма. Наиболее ярким
примером является транспорт ионов Na+, который осуществляется при
участии фермента Na, К—АТФазы, расходующей энергию АТФ. После освобождения от
связи с переносчиком глюкоза поступает в цитоплазму, достигает базальной
плазматической мембраны и перемещается через нее с помощью механизма
облегченной диффузии.
Белки и аминокислоты. Ультрафильтрация приводит к тому,
что в просвет нефрона поступают неэлектролиты и электролиты. В отличие от
электролитов которые, проникнув через апикальную мембрану, в неизменном виде
достигай ют базальной плазматической мембраны и транспортируются в кровь,
перенос белка обеспечивается иным механизмом, получившим название пиноцитоз.
Молекулы профильтровавшегося белка адсорбируются на поверхностной мембране
клетки, мембрана впячивается внутрь клетки с образованием пиноцитозной вакуоли.
Эта вакуоль движется в сторону базальной части клетки; в околоядерной области,
где локализован пластинчатый комплекс (аппарат Гольджи) они могут сливаться с
лизосомами, в которых высока активность ряда протеолитических ферментов. В
лизосомах захваченные белки в результате ферментативного гидролиза расщепляются
до аминокислот и удаляются в кровь через базальную плазматическую мембрану.
Профильтровавшиеся в клубочках аминокислоты почти полностью
реабсорбируются клетками проксимального канальца. В люминальной мембране
имеется не менее четырех раздельных механизмов транспорта аминокислот из
просвета канальца в кровь: специальные системы реабсорбции для нейтральных,
двуосновных, дикарбоксильных аминокислот и иминокислот (содержат в молекуле
двухвалентную иминогруппу =NH). Каждая из этих систем обеспечивает всасывание
нескольких аминокислот только одной группы. Так например, система реабсорбции
двуосновных аминокислот участвует во всасывании лизина, аргинина, орнитина и,
возможно, цистина. При введении в кровь избытка одной из указанных выше
аминокислот начинается усиленная экскреция остальных аминокислот только этой
группы. Системы транспорта отдельных групп аминокислот контролируются'
раздельными генетическими механизмами. Описаны наследственные заболевания,
одним из проявлений которых служит увеличенная экскреция определенных групп
аминокислот.
Недавно были получены данные, что в почечных канальцах могут
реабсорбироваться дипептиды и трипептиды в неизмененном виде. Пептидные
гормоны, фильтруемые в почечных клубочках, частично гидролизуются и
возвращаются в кровь в виде аминокислот, частично экскретируются с мочой.
Выделение с мочой слабых кислот и оснований зависит от их ультрафильтрации
в клубочках, реабсорбции и секреции в проксимальных канальцах, а также от
«неионной диффузии», влияние которой особенно сказывается в дистальных
канальцах и собирательных трубках. Эти соединения могут существовать в
зависимости от рН среды в двух формах: неионизированной и ионизированной.
Клеточные мембраны более проницаемы для неионизированных веществ. Многие слабые
кислоты с большой скоростью экскретируются с щелочной мочой, а слабые
основания, напротив, с кислой. У оснований степень ионизации увеличивается в
кислой среде, но уменьшается в щелочной. В неионизированном состоянии эти
вещества растворимы в липидах и проникают в клетки, а затем в плазму крови, т.
е. реабсорбируются. Если в канальцевой жидкости значение рН сдвинуто в кислую сторону,
основания ионизированы и преимущественно экскретируются с мочой. Так, например,
никотин является слабым основанием, ионизированным на 50% при рН 8,1, он в 3—4
раза быстрее экскретируется с кислой мочой (рН около 5), чем при щелочной
реакции (рН 7,8). Неионная диффузия влияет на выделение почкой аммония, ряда
лекарственных препаратов.
Электролиты. Всасывание профильтровавшихся в клубочках ионов Na+,
Сl— и НСО3—
требует наибольших энерготрат в клетках нефрона. У человека в 1 сут
реабсорбируются около 24 330 ммоль натрия, 19 760 ммоль хлора, 4888 ммоль
бикарбоната, а выделяется с мочой 90 ммоль натрия, 90 ммоль хлора, менее 2
ммоль бикарбоната. Транспорт натрия является первично—активным, т. е. именно на
его перенос расходуется энергия клеточного обмена. Ведущую роль в этом процессе
играет Na, К—АТФаза. В проксимальном канальце у млекопитающих реабсорбируется
около 2/3 профильтровавшегося натрия. Обратное всасывание Na+ в этом
канальце происходит против небольшого градиента, и его концентрация в
канальцевой жидкости остается такой же, как и в плазме крови. В проксимальном
канальце реабсорбируются все остальные ионы. Как отмечалось выше, из—за высокой
проницаемости стенки этого канальца для воды жидкость в просвете нефрона
остается изоосмотичной плазме крови.
Ранее считали, что в проксимальном сегменте нефрона
происходит обязательная (облигатная) реабсорбция, т. е. при всех
условиях всасывание ионов Na+, Сl—, воды является постоянной
величиной. Напротив, в дистальных извитых канальцах и собирательных трубках реабсорбция
ионов и воды может регулироваться, ее величина меняется в зависимости от
функционального состояния организма. Результаты последних исследований
указывают на то, что под влиянием импульсов, поступающих по эфферентным нервным
волокнам к почке, и при действии физиологически активных веществ (например,
одного из натрийуретических гормонов) регулируется реабсорбция натрия и в
проксимальном отделе нефрона. Это особенно отчетливо выявляется при увеличении
объема внутрисосудистой жидкости, когда уменьшение реабсорбции в проксимальном
канальце способствует усилению экскреции ионов и воды, а тем самым
восстановлению объема крови.
В результате реабсорбции в проксимальном канальце
большинства компонентов ультрафильтрата и воды объем первичной мочи резко уменьшается
и в начальный отдел петли Генле у млекопитающих поступает около l/з
профильтровавшейся в клубочках жидкости. В петле Генле всасывается до 25%
натрия, поступившего в нефрон при фильтрации, в дистальном извитом канальце —
около 9%; меньше 1% натрия реабсорбируется в собирательных трубках или
экскретируется с мочой. В конечных отделах канальцев концентрация натрия может
снижаться до 1 ммоль/л по сравнению с 140 ммоль/л в клубочковом фильтрате. В
дистальном сегменте нефрона и собирательных трубках в отличие от проксимального
сегмента всасывание происходит против высоких концентрационного и
электрохимического градиентов.
|
|
|
Рис. 13.9 Мембранные механизмы транспорта Na+ в клетках различных
отделов нефрона В
базальных мембранах всех типов клеток содержится Na, К—АТФаза, обеспечивающая обмен
ионов Na+ на ионы К+. В люминальной мембране локализована система котранспорта
Na+ и глюкозы (G), натриевые каналы, система котранспорта некоторых других
ионов; стрелками указаны участки нефрона, где находятся клетки
соответствующих типов. |
|
|
|
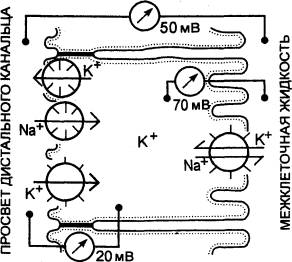
Рис. 13.10 Транспорт Na+ и К+
клеткой дистального извитого канальца |
Клеточные механизмы реабсорбции Na+, как и
других ионов, могут существенно отличаться в разных отделах нефрона (рис. 13.9).
В клетках проксимального канальца поступление натрия через люминальную мембрану
внутрь клетки обеспечивается рядом механизмов. Оно может быть связано с обменом
Nа+ на протоны (Na+/H+, а также с деятельностью
натрийзависимых переносчиков аминокислот и глюкозы. В люминальной мембране
клеток толстого восходящего отдела петли Генле поступление иона Na+
в клетку происходит одновременно с ионом К+ и двумя ионами Сl—; эта система блокируется со стороны
просвета канальца фуросемидом. В дистальном извитом канальце ведущее
значение имеет прохождение иона Na+ по натриевому каналу,
специфическим блокатором которого является амилорид. Во всех случаях
поступившие внутрь клетки ионы натрия удаляются из нее Na, К—АТФазой,
локализованной в базальной плазматической мембране.
Таким образом, молекулярные механизмы реабсорбции ионов
натрия не одинаковы в разных участках нефрона. Это определяет отличие скорости
реабсорбции и способов регуляции переноса натрия.
Электрофизиологические исследования клеток нефрона подтверждают
высказанные выше представления о пассивном и активном компонентах системы
реабсорбции натрия. При реабсорбции натрий вначале входит в клетку эпителия
канальца пассивно по натриевому каналу мембраны, обращенной в сторону просвета
канальца; внутренняя часть клетки заряжена отрицательно, и поэтому положительно
заряженный Na+ движется в клетку по градиенту потенциала. Натрий
направляется в сторону базальной плазматической мембраны, в которой имеется
натриевая помпа, выбрасывающая его в межклеточную жидкость (рис. 13.10).
Регуляция реабсорбции и секреции ионов в почечных канальцах. В регуляции реабсорбции натрия
участвуют эфферентные нервные волокна, подходящие к почке, и некоторые гормоны
(рис. 13.11). Вазопрессин усиливает всасывание натрия в клетках толстого
восходящего отдела петли Генле. Механизм этого эффекта основан на
внутриклеточном действии цАМФ. Другим стимулятором реабсорбции натрия является альдостерон,
который увеличивает транспорт Na+ в клетках дистальных почечных
канальцев. Из внеклеточной жидкости этот гормон проникает через базальную
плазматическую мембрану в цитоплазму клетки и соединяется с рецептором.
Возникший комплекс поступает в ядро, где образуется комплекс альдостерона со
стереоспецифичным для него хроматином.
В связывании альдостерона, по—видимому, участвует
негистонный хромосомный белок, молекулы альдостерона связываются ядром почечной
клетки. В ядре стимулируется транскрипция определенного участка генетического
кода, синтезированная мРНК переходит в цитоплазму и активирует образование
белков, необходимых для увеличения транспорта Na+.
Альдостерон стимулирует образование компонентов натриевого
насоса (Na, К—АТФазы), ферментов его энергетического обеспечения, а также
веществ, облегчающих вход Na+ в клетку из просвета канальца. В
обычных физиологических условиях одним из факторов, ограничивающих реабсорбцию
натрия, является низкая проницаемость апикальной плазматической мембраны.
Возрастание числа натриевых каналов мембраны (или времени их открытого
состояния) увеличивает вход натрия в клетку и повышает в ней его содержание,
что стимулирует активный перенос натрия.
|
|
|
Рис.13.11 Место действия гормонов и медиаторов в различных сегментах почечного
канальца I — натрийуретический гормон, 2 — катехоламины,
3 — глюкокортикоиды, 4 —
паратгормон, 5— кальцитонин, 6 —
вазопрессин, 7 — альдостерон. |
Уменьшение реабсорбции натрия достигается под влиянием так
называемого натрийуретического гормона, выработка которого возрастает при
увеличении объема циркулирующей крови, повышении объема внеклеточной жидкости в
организме. Структура и место секреции этого гормона установлены лишь в
последние годы, хотя мысль о его существовании была высказана в конце 50—х гг.
Оказалось, что таких факторов несколько: один из них выделяется в предсердии,
другой — в гипоталамической области; ряд натрийуретических веществ выделен из
некоторых других органов. В настоящее время значение каждого из них в реальных
процессах регуляции обмена натрия еще не ясно.
Реабсорбция ионов СL— происходит в некоторых частях нефрона с
помощью иных механизмов, чем реабсорбция Na+, что дает возможность раздельно
регулировать выделение натрия и хлора почкой. В начальных частях проксимального
отдела нефрона его стенка непроницаема для ионов Сl—, ионы Na+ всасываются вместе с НСО3—.
В результате концентрация Сl— возрастает со 103 до 140 ммоль/л. В конечных участках
проксимального канальца зона межклеточных соединений проницаема для ионов Сl—. Так как концентрация Сl— в канальцевой жидкости стала выше,
чем в плазме крови, то СL— по концентрационному градиенту движется в
межклеточную жидкость и кровь. За ионами хлора следуют и ионы натрия.
Механизм реабсорбции ионов хлора в клетках толстого
восходящего отдела петли Генле иной. В люминальной мембране имеется
своеобразный молекулярный механизм транспорта ионов Сl—, одновременно с которыми
всасываются ионы Na+ и К+.
В дистальном извитом канальце и собирательных трубках активно
транспортируются через клетки ионы Na+, за ними по электрохимическому
градиенту следуют ионы Сl—.
Различие способов реабсорбции ионов хлора имеет важное
значение для понимания многообразия молекулярных механизмов реабсорбции ионов.
Особенно следует подчеркнуть, что для этого процесса имеет значение не только
отличие свойств ионных каналов и ионных переносчиков в люминальной мембране
клеток, но и своеобразие свойств зоны клеточных контактов. В начальных участках
нефрона они непроницаемы для неэлектролитов и ионов Сl—, последующие части проксимального
канальца обладают высокой проницаемостью для ионов Сl—. В дистальном сегменте нефрона и
собирательных трубках зона клеточных контактов очень плохо пропускает
растворенные вещества, что обеспечивает возможность их экскреции почкой.
В почечных канальцах реабсорбируются
калий, кальций, магний, фосфаты, сульфаты, микроэлементы. Почки являются
важнейшим эффекторным органом в системе ионного гомеостаза. Новейшие данные
свидетельствуют о существовании в организме систем регуляции баланса каждого из
ионов. Для некоторых из ионов уже описаны специфические рецепторы, например натриорецепторы.
Появились и первые данные о рефлекторной регуляции транспорта ионов в почечных
канальцах, включающей рецепторы, центральные аппараты и эфферентные пути
передачи сигнала почке.
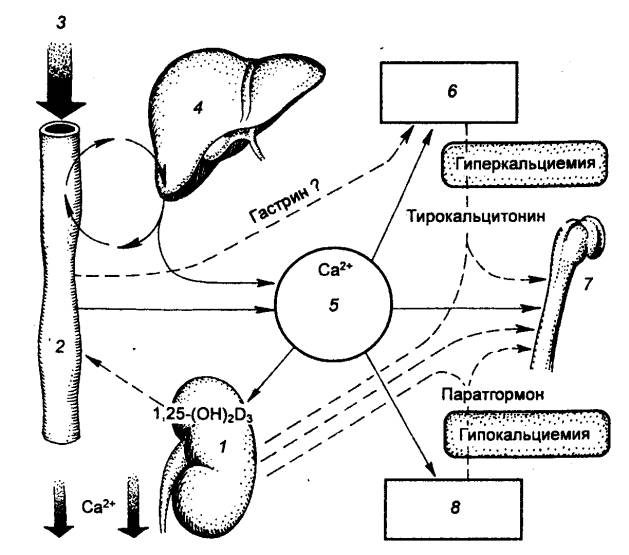
Регуляцию реабсорбции ионов Са2+
в почечных канальцах осуществляет ряд гормонов (рис. 13.12). При уменьшении
концентрации кальция в крови паращитовидные
|
|
|
Рис.
13.12 Регуляция обмена кальция 1 — почка, 2 — кишка, 3 — пища, 4 — печень, 5 — плазма крови, 6 —
щитовидная железа, 7 — кость,
8 — паращитовидная железа;
пунктирными стрелками обозначено изменение реакции при увеличении или
уменьшении концентрации кальция в крови. |
железы выделяют паратгормон,
который способствует нормализации уровня Са2+ в крови за счет
увеличения его реабсорбции в почечных канальцах и повышения резорбции кости.
При гиперкальциемии стимулируется выделение в кровь гормона щитовидной железы —
тиреокальцитонина, который снижает концентрацию кальция в крови и
способствует увеличению его экскреции почкой. Важную роль в регуляции обмена Са2+
играет активная форма витамина D3— 1,25 (ОН)2—D3. В почечных канальцах
регулируется уровень реабсорбции магния, хлора, сульфатов и других ионов.
В современной физиологической
литературе, касающейся деятельности почек, термин секреция имеет два
значения. Первое из них описывает процесс переноса вещества через клетки из
крови в просвет канальца в неизменном виде, что увеличивает скорость экскреции
вещества почкой. Второе — выделение из клетки в кровь или в просвет канальца
синтезированных в почке физиологически активных веществ (например,
простагландины, брадикинин и др.) или экскретируемых веществ (например, гиппуровая
кислота). В этом разделе основное внимание будет уделено описанию процесса
секреции в первом значении этого слова.
Секреция органических и неорганических веществ — один из
важных процессов, обеспечивающих процесс мочеобразования. У рыб некоторых видов
в почке отсутствуют клубочки. В таких случаях секреция играет ведущую роль в
деятельности почки. В почках большинства других классов позвоночных, в том
числе и у млекопитающих, секреция обеспечивает выделение из крови в просвет
канальцев дополнительных количеств некоторых веществ, которые могут
фильтроваться ив почечных клубочках.
Таким образом, секреция ускоряет выделение почкой некоторых
чужеродных веществ, конечных продуктов обмена, ионов. В почке у млекопитающих
секретируются органические кислоты (пенициллин, парааминогиппуровая кислота —
ПАГ, диодраст, мочевая кислота), органические основания (холин, гуанидин),
неорганические вещества (калий). Почка гломерулярных и агломерулярных морских
костистых рыб способна к секреции ионов магния, кальция, сульфатов. Различаются
места секреции разных веществ. В почке всех позвоночных местом секреции
органических кислот и оснований служат клетки проксимального сегмента нефрона,
особенно его прямой части, секреция калия преимущественно происходит в клетках
дистального извитого канальца и собирательных трубок.
Механизм процесса секреции органических кислот. Рассмотрим этот процесс на примере
выделения почкой ПАГ. После введения в кровь ПАГ ее секреция почкой нарастает и
очищение от нее крови значительно превышает величину очищения крови от
одновременно введенного инулина. Это означает, что ПАГ не только фильтруется в
клубочках, но и помимо клубочков в просвет нефрона поступают значительные ее
количества. Экспериментально было показано, что такой процесс обусловлен секрецией
ПАГ из крови в просвет проксимальных отделов канальцев. В мембране клетки этого
канальца, обращенной к межклеточной жидкости, имеется переносчик
(котранспортер), обладающий высоким сродством к ПАГ. В присутствии ПАГ
образуется комплекс переносчика с ПАГ, который перемещается в мембране и на ее
внутренней поверхности распадается, высвобождая ПАГ в цитоплазму, а переносчик
приобретает снова способность перемещаться к внешней поверхности мембраны и
соединяться с новой молекулой ПАГ. Механизм секреции органических кислот
включает ряд этапов. В базальной плазматической мембране имеется Na+, K+—АТФаза, которая удаляет из клетки
ионы Na+ и способствует поступлению в клетку ионов К+. Более низкая
концентрация в цитоплазме ионов Na+ позволяет поступать внутрь клетки
ионам Na+ по градиенту концентрации при участии натриевых
котранспортеров. Один из типов такого котранспортера способствует поступлению
через базальную плазматическую мембрану α—кетоглутарата и Na+. В этой же мембране имеется
анионный обменник, который удаляет из цитоплазмы α—кетоглутарат в обмен на поступающий
из межклеточной жидкости в клетку парааминогиппурат (ПАГ), диодраст или
некоторые иные органические кислоты. Это вещество движется по клетке в сторону
люминальной мембраны и через нее проходит в просвет канальца по механизму
облегченной диффузии.
Угнетение дыхания цианидами, разобщение дыхания и
окислительного фосфорилирования динитрофенолом снижает и прекращает секрецию. В
обычных физиологических условиях уровень секреции зависит от числа переносчиков
в мембране. Секреция ПАГ возрастает пропорционально увеличению концентрации ПАГ
в крови до тех пор, пока все молекулы переносчика не насытятся ПАГ.
Максимальная скорость транспорта ПАГ достигается в тот момент, когда количество
ПАГ, доступное для транспорта, равно количеству молекул переносчика, которые
могут образовывать комплекс с ПАГ. Эта величина определяется как максимальная
способность к транспорту ПАГ — Ттран (см. рис. 13.7). Поступившая в
клетку ПАГ движется по цитоплазме к апикальной мембране и через нее специальным
механизмом выделяется в просвет канальца.
Секреция органических оснований. Этот процесс (например, секреция
холина), подобно выведению органических кислот, происходит в проксимальном
сегменте нефрона и характеризуется определенной величиной максимального
транспорта (Т т). Системы секреции органических кислот и оснований
функционируют независимо друг от друга. Это было показано экспериментально,
когда животным вводили пробенецид — вещество, угнетающее секрецию органических кислот.
В таком опыте секреция органических оснований не нарушалась.
Для определения секреции в почечных канальцах рассчитывают
очищение крови от данного вещества и очищение от инулина. Если клиренс
исследуемого вещества превышает клиренс инулина, это указывает на секрецию в
канальцах. При одновременном определении в плазме крови исследуемого вещества
(а) и инулина (In) достаточно рассчитать отношение их концентрационных
показателей Ua/Рa: Uin/Pin, так как объем выделяемой мочи
будет одинаковым.
Если это отношение больше единицы, то вещество
секретируется, если меньше — реабсорбируется. Однако это упрощенная оценка
системы транспорта веществ в нефроне. Некоторые из них, например ионы калия и
мочевая кислота, могут подвергаться и реабсорбции, и секреции. Поэтому наряду с
измерением концентрационных показателей необходимо изучение особенностей
обработки исследуемых веществ в отдельных частях почечных канальцев.
Секреторную функцию проксимальных отделов нефрона измеряют с помощью
веществ, которые выделяются из организма главным образом посредством
канальцевой секреции (например, ПАГ, диодраст). Одно из этих веществ вводят в
кровь вместе с инулином, который служит для одновременного измерения
клубочковой фильтрации. Величину транспорта (Т) органического вещества (ПАГ)
при секреции (s) из крови в просвет канальца
определяют по разности между выделением этого вещества почкой (UранV ) и его
фильтрацией в клубочках (CinPран) : Тsрaн = upahv — CinPpан. При условии полного насыщения секреторного аппарата ПАГ определяется
величина максимального канальцевого транспорта ПАГ — ТтРАН. У
человека ТтРАН составляет 79 мг/мин при расчете на 1,73 м2
поверхности тела.
Способность клеток проксимальных канальцев практически
полностью извлекать из околоканальцевой жидкости и, соответственно, из крови
околоканальцевых капилляров такие органические кислоты, как ПАГ и диодраст,
была использована для измерения эффективного почечного кровотока — кровоснабжения
коры почки. Непрямой метод измерения величины почечного кровотока основан
на способности клеток проксимальных почечных канальцев секретировать ПАГ и
диодраст столь эффективно, что при невысокой их концентрации в артериальной
крови последняя полностью очищается от этих веществ при однократном прохождении
через почку. Очищение от ПАГ (СРАН) эквивалентно плазмотоку и
определяется по формуле ( UРАН
/ РРАН) V, где U и Р— концентрация ПАГ в моче
и плазме крови, V — диурез, СРАН — величина эффективного почечного
плазмотока, т. е. то количество плазмы, которое протекает по сосудам коры почки
и омывает клетки проксимального сегмента нефрона. Так как эритроциты не
содержат ПАГ, для расчета величины эффективного почечного кровотока (ERBF — англ. Effective Renal Blood Flow) необходимо учитывать соотношение
между эритроцитами и плазмой крови (показатель гематокрита Ht): ERBF == СРАН/(1 — Ht).
Общий кровоток и плазмоток через почки может быть рассчитан
в том случае, если известно, сколько ПАГ не удаляется клетками канальцев. Так
как считают, что ПАГ полностью извлекается из крови, протекающей в коре почки,
то наличие в почечной вене небольшого количества ПАГ обусловлено той частью
крови, которая минует кору почки и поступает в сосуды мозгового вещества. Доля
кровотока через все мозговое вещество мала по сравнению с общим почечным
кровотоком и составляет от 7 до 9%, а кровоток во внутреннем мозговом веществе
(почечный сосочек) равен лишь 1%.
Секреция неорганических веществ. Клетки почечных канальцев способны
не только к секреции органических кислот и оснований, но и некоторых
неорганических веществ. В почке проходных и морских костистых, а также хрящевых
рыб могут секретироваться ионы калия, магния, кальция, сульфаты. В почках
млекопитающих секретируются ионы К+ и H+.
Транспорт калия в нефроне отличается от переноса натрия тем, что K.+
подвергается не только реабсорбции, но и секретируется в почке клетками
конечных отделов нефрона и собирательных трубок.
При реабсорбции калий поступает в клетку нефрона из просвета
канальца. В клетке концентрация K+ выше, чем в
околоканальцевой жидкости, и калий диффундирует из клетки через базальную
плазматическую мембрану в межклеточное вещество, а затем уносится кровью. При
секреции калий вначале поступает в клетку из межклеточной жидкости в обмен на
натрий с помощью Na, К—насоса (Na, К—АТФаза), который одновременно удаляет Na+
из клетки. Тем самым поддерживается высокая внутриклеточная концентрация К+.
При избытке калия в организме начинается его секреция
клетками в просвет канальца, зависящая от ряда факторов, прежде всего от
степени возрастания проницаемости для К+ мембраны клетки, обращенной
в просвет канальца. В ней открываются «каналы», по которым калий по градиенту
концентрации может выходить из клетки. Скорость секреции К+ зависит
от градиента электрохимического потенциала на апикальной мембране клетки: чем
больше ее электроотрицательность, тем выше уровень секреции К+.
Поэтому введение слабореабсорбируемых анионов, например сульфатов, увеличивает
секрецию К+.
Таким образом, секреция калия
зависит от его внутриклеточной концентрации, проницаемости для калия апикальной
мембраны и градиента электрохимического потенциала на мембране. В регуляции
секреции К+ важное значение имеет гормон коры надпочечника альдостерон,
который увеличивает реабсорбцию натрия и одновременно усиливает секрецию калия.
Почти весь профильтровавшийся в клубочках калий реабсорбируется в отделах
нефрона, расположенных до дистального извитого канальца. Калий, выделяемый с
мочой, секретируется в конечных частях дистального сегмента нефрона и
собирательных трубках.
13.6.5. Синтез веществ в почке
В почке образуются некоторые
вещества, выделяемые в мочу (например, гиппуровая кислота, аммиак), а также
поступающие в кровь (ренин, простагландины, глюкоза, появляющаяся при
глюконеогенезе в почке, и др.). Гиппуровая кислота синтезируется в
клетках канальцев из бензойной кислоты и гликокола. В опытах на изолированной
почке было показано, что при введении в почечную артерию раствора бензойной
кислоты и гликокола в моче появляется гиппуровая кислота. В клетках канальцев
при дезаминировании аминокислот, главным образом глутамина, из аминогрупп
образуется аммиак. Он поступает преимущественно в мочу, но частично
проникает и через базальную плазматическую мембрану в кровь: в почечной вене
аммиака больше, чем в почечной артерии.
13.6.6. Осмотическое разведение и концентрирование мочи
Почки практически всех пресноводных
и наземных позвоночных способны выделять мочу, имеющую меньшее, чем кровь, осмотическое
давление. Это дает им возможность экскретировать избыток воды и повышать
сниженную осмоляльность крови до нормальных значений. При дефиците воды, когда
осмотическое давление крови может быть повышено, необходимо экономить воду и
экскретировать осмотически активные вещества в виде гиперосмотической мочи.
Такой способностью обладают только млекопитающие и птицы, в почках которых
имеется мозговое вещество. Чем более развито мозговое вещество в почке,
чем более сформирована его внутренняя часть, в которой находятся тонкие отделы
петель Генле, тем эффективнее осуществляется осмотическое концентрирование
мочи. Так, у морской свинки всего 5% нефронов имеют длинные петли Генле, у
белых крыс их 28%, а у больших песчанок (Rhombomys opimus), обитающих в пустыне, таких нефронов 100%. В почке
морской свинки внутреннее мозговое вещество слабо развито, у большой песчанки
почечный сосочек очень длинный, свисающий в почечную лоханку. Почки большой
песчанки способны вырабатывать мочу, осмотическое давление которой превышает
100 атм.
Осмотическое концентрирование. В зависимости от состояния водного
баланса организма почки млекопитающих и птиц выделяют разведенную или концентрированную
мочу. В процессе осмотического концентрирования мочи в почке принимают
участие все отделы канальцев, сосуды мозгового вещества, межклеточная ткань
(рис. 13.13). В почках у млекопитающих 2/3 ультрафильтрата, образовавшегося в
клубочках, реабсорбируется к концу проксимального сегмента. Оставшаяся в
канальцах жидкость содержит осмотически активные вещества в такой же
концентрации, как и плазма крови, хотя и отличается от нее по составу
вследствие реабсорбции органических веществ и ионов. Далее канальцевая жидкость
переходит из коркового слоя почки в мозговое вещество — в нисходящий отдел петли
Генле — и движется до вершины почечного сосочка, где каналец изгибается на 180°
и моча переходит в восходящий отдел
|
|
|
Рис. 13.13 Процесс осмотического разведения (А) и концентрирования (Б) мочи I — корковое вещество, II — наружное мозговое вещество, III — внутреннее мозговое вещество
почки; 1 — клубочек, 2 — проксимальный извитой канадец, 3 — нисходящая тонкая ветвь, 4 — восходящая тонкая ветвь, 5 — восходящая толстая ветвь петли Генле, 6 — дистальный извитой канадец, 7 — собирательная трубка
коркового слоя почки, 8 —
собирательная трубка наружного мозгового вещества почки, 9 — собирательная трубка
внутреннего мозгового вещества почки; цифрами указана осмоляльность жидкости
просвета канальца и межклеточного вещества; стрелками из просвета канальца
обозначена реабсорбция воды (Н2О), неэлектролитов (Нэ,
электролитов (Э), мочевины (М); сплошными стрелками — активный транспорт;
пунктирными — за счет диффузии. |
петли, расположенный параллельно ее нисходящему
отделу. В нем жидкость течет в направлении от вершины сосочка к коре почки.
Функциональное значение различных
отделов петли неоднозначно. Когда жидкость из проксимального канальца поступает
в тонкий нисходящий отдел петли Генле, она попадает в зону почки, в
межклеточном веществе которой концентрация осмотически активных веществ выше,
чем в коре почки. Это повышение осмолярной концентрации в наружной зоне
мозгового вещества обусловлено деятельностью толстого восходящего отдела петли
Генле. Его стенка непроницаема для воды, а клетки транспортируют ионы СL—
и Na+ в межклеточное вещество. Стенка
нисходящего отдела петли проницаема для воды, и вода всасывается из просвета
канальца в окружающую межуточную ткань почки по осмотическому градиенту.
Осмотическая концентрация жидкости в
восходящем отделе петли на границе коры и мозгового вещества составляет около
200 моем, т. е. она ниже, чем в плазме крови и ультрафильтрате. Поступление
ионов хлора и натрия в межклеточное вещество наружного мозгового слоя
увеличивает его осмолярную концентрацию до 400 моем. На такую же величину
растет и осмолярная концентрация жидкости, находящейся в просвете нисходящего
отдела петли. Через его проницаемую для воды стенку в межуточную ткань по
осмотическому градиенту переходит вода, а осмотически активные вещества
остаются в просвете этого отдела канальца.
Чем дальше от коры по продольной оси
почечного сосочка исследуют жидкость в нисходящем колене петли, тем выше
оказывается ее осмолярная концентрация. В соседних смежных участках нисходящего
отдела петли имеется лишь небольшое нарастание осмотического давления, но по
длиннику почечного сосочка (внутреннего мозгового вещества) осмолярная
концентрация постепенно растет от 300 мосм/л почти до 1450 мосм/л у человека
или почти до 4500 мосм/л у большой песчанки.
На вершине почечного сосочка
осмолярная концентрация жидкости в петле Генле возрастает в несколько раз,
объем ее уменьшается. При дальнейшем движении жидкости по восходящему отделу
петли продолжается реабсорбция ионов СL— и Na+, вода же
остается в просвете канальца. В начальные отделы дистального извитого канальца
всегда поступает гипотоническая жидкость, концентрация осмотически активных
веществ в которой менее 200 моем/л.
В условиях дефицита воды в организме
гипофиз усиливает секрецию антидиуретического гормона (аргинин—вазопрессин,
АДГ), что увеличивает проницаемость стенок конечных частей дистального сегмента
и собирательных трубок для воды. Из гипотонической жидкости по осмотическому
градиенту реабсорбируется вода, осмолярная концентрация жидкости в этом отделе
увеличивается до 300 мосм/л, т. е. жидкость в просвете канальца становится
изоосмотичной крови в системном кровотоке и коре почки.
Окончательное осмотическое
концентрированно мочи
наступает в собирательных трубках. Они расположены параллельно канальцам петли
Генле в мозговом веществе почки. Как отмечалось выше, в межклеточной жидкости
мозгового вещества почки возрастает осмолярная концентрация. Вследствие этого
из жидкости собирательных трубок реабсорбируется вода и концентрация мочи в них
увеличивается, уравновешиваясь со все повышающейся концентрацией осмотически
активных веществ во внутреннем мозговом веществе почки. В конечном счете
выделяется гиперосмотическая моча, в которой максимальная концентрация
осмотически активных веществ может быть равна осмолярной концентрации
межклеточной жидкости на вершине почечного сосочка.
В наружной зоне мозгового вещества
почки повышение осмолярности главным образом основано на транспорте ионов Na+
и СL—. Увеличение осмолярной концентрации во внутренней зоне
мозгового вещества почки зависит от нескольких механизмов, обеспечивающих
накопление ионов натрия, хлора и мочевины. Особую роль для осмотического
концентрирования играет в этой части почки аккумуляция мочевины, что
происходит следующим образом.
Стенка проксимального канальца
проницаема для мочевины, что приводит к реабсорбции до 50% профильтровавшейся
мочевины. Однако при извлечении жидкости из извитого дистального канальца
оказалось, что в нем содержание мочевины очень высоко.
Показано, что существует система
внутрипочечного кругооборота мочевины, участвующая в осмотическом
концентрировании мочи. В просвете собирательных трубок вследствие реабсорбции
воды концентрация мочевины повышается. АДГ увеличивает проницаемость
собирательных трубок в мозговом веществе не только для воды, но и для мочевины,
в результате она диффундирует в мозговое вещество почки. Мочевина проникает из
межклеточной жидкости в просвет прямого сосуда и тонкого отдела петли Генле.
Поднимаясь вместе с током жидкости
по направлению к коре почки по прямому сосуду, мочевина непрерывно участвует в противоточном
обмене, диффундирует в нисходящий отдел прямого сосуда и нисходящую часть
петли Генле. Вследствие этого происходит постоянное поступление мочевины во
внутреннее мозговое вещество, а также ионов СL— и Na+,
реабсорбируемых клетками толстого восходящего отдела петли Генле и
собирательных трубок. Эти вещества удерживаются в мозговом веществе благодаря
деятельности противоточной системы прямых сосудов и петель Генле, что в
конечном счете обеспечивает повышение осмотической концентрации во внутреннем
мозговом веществе почки. Вслед за увеличением осмолярности межуточной ткани,
окружающей собирательные трубки, возрастает и реабсорбция воды из них,
повышается эффективность осморегулирующей функции почки. Увеличение
проницаемости канальцевой стенки для мочевины в присутствии АД Г позволяет
понять, почему при снижении мочеотделения уменьшается очищение от мочевины.
Прямые кровеносные сосуды мозгового
вещества почки, подобно канальцам петли Генле, также образуют противоточную
систему, играющую очень важную роль в осмотическом концентрировании.
Благодаря параллельному расположению прямых сосудов и петель Генле обеспечивается
эффективное кровоснабжение мозгового вещества почки, но не происходит вымывания
осмотически активных веществ, так как в крови прямых сосудов наблюдаются такие
же изменения осмотической концентрации, как и в тонком нисходящем отделе петли
Генле. При движении крови по направлению к вершине почечного сосочка в ней
постепенно возрастает осмотическая концентрация, а во время ее обратного
движения к коре почки диффундирующие через сосудистую стенку соли и другие
растворенные вещества переходят в межклеточную ткань.
Тем самым сохраняется градиент
концентрации осмотически активных веществ внутри почки и прямые сосуды
функционируют как противоточная система. Скорость движения крови по прямым
сосудам влияет на количество удаляемых из мозгового вещества ионов натрия,
хлора и мочевины, участвующих в создании осмотического градиента и оттоке
реабсорбируемой воды.
Для количественной оценки
концентрационной способности почки в условиях экономии воды используют два
параметра: индекс осмотического концентрирования, показывающий, во
сколько раз моча более осмотически концентрирована, чем кровь, и объем
реабсорбированной осмотически свободной воды. Физиологическое значение
этого показателя, имеющего очень важное значение, требует специального
объяснения.
Образование мочи всегда происходит
из жидкости, имеющей такую же общую концентрацию осмотически активных веществ,
как и плазма крови. Так как выделение почкой осмотически активных веществ равно
произведению диуреза (V, мл/мин) на концентрацию осмотически активных веществ в
моче (Uosm,
мосм/л), то очищение плазмы крови от осмотически активных веществ (Cosm) равно:
Cosm = UosmV/Posm
где Posm — концентрация осмотически активных веществ в плазме
крови, мосм/л. Величина Cosm характеризует тот условный объем плазмы
крови, который очистился от осмотически активных веществ в течение 1 мин. Иными
словами, если выделяется моча, имеющая такую же осмотическую концентрацию, как
и плазма крови, то Cosm = V и почка только уменьшает объем жидкости в организме, не участвуя в осморегуляции.
Однако при
обезвоживании почка выделяет мочу более осмотически кок центрированную, чем
кровь. Воду, выделяемую с мочой, условно можно разделить на две фракции. Одна
из них содержит растворенные вещества в той же концентрации, что и плазма крови,
т. е. равна Cosm» другая представляет собой чистую, свободную от веществ воду.
Ее называют осмотически свободной водой (СН2О).
Следовательно, сказанное можно представить в виде такой формулы:
V = Cosm + H2O
Образование гипотонической мочи. При потреблении больших количеств
воды почки выделяют гипотоническую мочу и СН2О представляет собой
положительную величину, при обезвоживании организма, напротив, отрицательную.
Это означает, что осмотически свободная вода не экскретируется, а всасывается в
канальцах в кровь. Выше был подробно описан механизм осмотического
концентрирования мочи. Величина реабсорбции (мл/мин) осмотически свободной воды
(ТсН2О) численно равна СН2О но с обратным
знаком: ТсН2О=С. Существенно, что эта величина является
константной для данного вида. Так, у человека при дегидратации максимальное
значение реабсорбции осмотически свободной воды не превышает 5 мл/мин при
нормальном значении клубочковой фильтрации.
При поступлении избытка воды в
организм почки начинают выделять большие объемы гипотонической мочи. Переход от
экономии к экскреции воды сопровождается снижением клубочковой фильтрации в
юкстамедуллярных нефронах и ее увеличением в клубочках других популяций
нефронов.
При водном диурезе относительная
проксимальная реабсорбция ионов и воды не изменяется, а в дистальный сегмент
нефрона поступает такое же количество жидкости, как и при дегидратации.
Осмолярность мозгового вещества почки при водном диурезе становится ниже, чем
при антидиурезе, а осмотическая концентрация жидкости, поступающей в дистальный
сегмент нефрона, такая же — приблизительно 200 мосм/л. При водном диурезе
стенка конечных отделов почечных канальцев остается водонепроницаемой, а из
протекающей мочи клетки продолжают реабсорбировать соли натрия; в результате
выделяется гипотоническая моча, концентрация осмотически активных веществ в
которой ниже 50 мосм/л. Проницаемость канальцев для мочевины низка, и она
экскретируется с мочой, не накапливаясь в мозговом веществе почки.
У человека на максимуме водного
диуреза мочеотделение может достигать 18 мл/мин. Очищение от осмотически
свободной воды в этом случае определяется по формуле Сизо = V— Cosm оно составляет у человека 13—15
мл/мин.
Таким образом, различие деятельности
петли Генле, конечных частей дистального сегмента и собирательных трубок
обусловливает способность почек при водной нагрузке выделять большие объемы
разведенной, гипотонической, мочи, а при дефиците воды в организме
экскретировать малые количества мочи, осмотически более концентрированной, чем
кровь. Исключительно развита способность почки осмотически концентрировать мочу
у некоторых пустынных грызунов, что позволяет им вообще не пить воду. У большой
песчанки, например, концентрация осмотически активных веществ в моче может
достигать 4000—4500 мосм/кг H2O, у ряда видов пустынных мышей она возрастает до 9000
мосм/кг H2O и
выше.
Собирательные трубки обеспечивают
реабсорбцию Na+, Cl— и других ионов против высокого градиента. Их основная функциональная особенность
состоит в том, что реабсорбция веществ происходит в небольших количествах, но
против наиболее значительного градиента, что и обусловливает резкие различия
концентрации ряда неорганических веществ в моче по сравнению с кровью.
13.6.7. Роль почек в осморегуляции и волюморегуляции
Осморегуляция. Почки являются основным эффекторным
органом системы осморегуляции. Они обеспечивают выделение избытка воды в виде
гипотонической мочи при поступлении воды в организм или экономят воду и экскретируют
мочу, гипертоническую по отношению к плазме крови, при обезвоживании. При
избыточном содержании воды в организме концентрация растворенных осмотически
активных веществ в крови снижается и ее осмотическое давление падает. Это
уменьшает активность центральных осморецепторов, расположенных в области
супраоптического ядра гипоталамуса, а также периферических осморецепторов,
имеющихся в печени, почке, селезенке и ряде других органов. Уменьшение
активности осморецепторов снижает секрецию антидиуретического гормона (АДГ)
нейрогипофизом и приводит к возрастанию выделения воды почкой (рис. 13.14).
|
|
|
Рис.
13.14 Участие почки в регуляции
водно—солевого обмена 1— ЦНС, 2 — гипоталамус, 3 — нейрогипофиз, 4 — почка, 5 — поджелудочная
железа, 6 — надпочечник; |
При обезвоживании организма, при
введении в сосудистое русло гипертонического раствора хлористого натрия
увеличивается концентрация осмотически активных веществ в плазме крови,
возбуждаются осморецепторы, стимулируются нейроны супраоптического ядра,
усиливается секреция АДГ, возрастает реабсорбция воды в канальцах, уменьшается
мочеотделение и выделяется осмотически концентрированная моча. Установлено, что
у человека в норме при осмоляльности крови около 280 мосм/кг H2O полностью прекращается секреция АДГ
и почка выделяет наибольшие количества воды. При обезвоживании когда
осмоляльность крови возрастает до 295 мосм/кг Н2О, секреция АДГ
достигает максимума и обнаруживается пик осмотического концентрирования мочи в
почке. В эксперименте показано, что секреция АДГ возрастает при раздражении не
только осморецепторов, но и специфических натриорецепторов. После
введения в область III желудочка мозга гипертонического раствора NaСl наступает антидиурез, а после
введения в ту же область гипертонических растворов сахара мочеотделение не
уменьшается.
Осморецепторы реагируют на сдвиги
концентрации осмотически активных веществ в плазме крови. При увеличении
осмоляльности плазмы крови на 1% (около 3 мосм/л) концентрация
аргинин—вазопрессина, являющегося антидиуретическим гормоном у человека и
многих других млекопитающих, возрастает на 1 пг/мл плазмы. Повышение
концентрации осмотически активных веществ в плазме на 1 мосм/кг воды вызывает
благодаря выделению АДГ увеличение осмотической концентрации мочи почти на 100
мосм/кг H2O, а переход от состояния водного диуреза до максимального осмотического
концентрирования мочи требует всего 10—кратного возрастания АДГ в крови — с 0,5
до 5 пг/мл.
Волюморецепция. Помимо информации от осморецепторов
и натриорецепторов уровень секреции АДГ зависит и от активности волюморецепторов,
реагирующих на изменение объема внутрисосудистой и внеклеточной жидкости.
Ведущее значение в регуляции секреции АДГ имеют те волюморецепторы, которые
реагируют на изменение напряжения сосудистой стенки. В первую очередь это
рецепторы левого предсердия, импульсы от которых передаются в ЦНС по
афферентным волокнам блуждающего нерва. При увеличении кровенаполнения левого
предсердия активируются волюморецепторы и угнетается секреция АДГ, тем самым
усиливается мочеотделение. В предсердии вырабатывается гормон, увеличивающий
выделение ионов Na+ почкой и получивший название атриальный
натрийуретический пептид.
Рассмотрим особенности реакции почки
при возбуждении волюморецепторов и осморецепторов. Активация только
волюморецепторов возникает в ответ на увеличение объема внутрисосудистой
жидкости при неизмененной концентрации в ней осмотически активных веществ. Это
приводит к повышению экскреции солей натрия и воды. Одновременная активация
волюморецепторов и осморецепторов может наступить при потреблении больших
количеств воды, в этом случае в основном усиливается выведение воды. Ведущую
роль в изолированном осморегулирующем рефлексе играет уменьшение секреции АДГ,
в результате снижается реабсорбция воды и усиливается ее экскреция.
Увеличение объема внеклеточной
жидкости, возрастание объема крови служат стимулом для волюморегулирующего
рефлекса. В эксперименте адекватным раздражителем системы регуляции объема
внеклеточной жидкости может служить введение в кровеносный сосуд больших
количеств изотоничного плазме крови физиологического раствора. Возрастание
притока крови к сердцу, растяжение стенки предсердия стимулируют
волюморецепторы и секрецию из клеток предсердия атриального натрийуретического
пептида. Под влиянием этого гормона усиливается выделение ионов натрия и воды
почкой.
Стимуляция волюморецепторов
рефлекторно изменяет характер импульсации иннервирующих почку симпатических
нервов и снижает реабсорбцию натрия и воды в канальцах. Возрастание объема
крови способствует растяжению афферентной артериолы клубочка. Это
сопровождается изменением активности юкстагломерулярного аппарата, уменьшением
секреции фермента ренина, благодаря чему снижается образование в крови из
ангиотензиногена ангиотензина I. После отщепления от него двух
аминокислот образуется ангиотензин II, который вызывает ряд эффектов, в
том числе стимулирует секрецию альдостерона. Когда снижается количество
ангиотензина, падает и поступление в кровь альдостерона, что приводит к
уменьшению реабсорбции натрия в канальцах. Активация волюморегулирующего
рефлекса снижает секрецию вазопрессина, тем самым уменьшается
реабсорбция воды и повышается ее выделение почкой.
Клеточное действие вазопрессина. Воздействие вазопрессина начинается
с активации рецепторов, расположенных на базальной и латеральных мембранах
клеток конечных частей дистального сегмента нефрона и собирательных трубок.
Существует два типа рецепторов вазопрессина: V1 и V2. Первый тип рецепторов после
взаимодействия с вазопрессином активирует образование таких вторичных
мессенджеров, как инозитолтрифосфат и диацилглицерол. Стимуляция
вазопрессином V2—рецепторов
завершается активацией фермента аденилатциклазы, в результате из АТФ
образуется вторичный мессенджер — цАМФ. Это физиологически активное
вещество внутри клетки вызывает ряд превращений, приводящих к увеличению
проницаемости для воды апикальной (люминальной) плазматической мембраны,
обращенной в просвет канальца.
В обычных условиях, когда в крови
нет вазопрессина, люминальная мембрана непроницаема для воды, клетка не
пропускает через себя воду и реабсорбция воды в собирательных трубках
практически не происходит. После секреции вазопрессина в кровь и стимуляции им
V2—рецепторов у внутренней поверхности базальной плазматической
мембраны образуется цАМФ. Этот вторичный мессенджер должен пересечь клетку и у
противоположной плазматической мембраны активировать ряд процессов,
завершающихся увеличением проницаемости для воды.
В цитоплазме клетки содержатся агрефоры.
— в них находятся так называемые «водные каналы» (аквапорины), которые
перемещаются к люминальной мембране и встраиваются в нее. Для осуществления
этого процесса необходимо участие микрофиламентов и микротрубочек. В конечном
счете цАМФ способствует встраиванию в люминальную мембрану агрегатов
внутримембранных частиц;
чем больше образуется цАМФ, тем
большая поверхность мембраны будет занята агрегатами частиц и выше становится
проницаемость для воды. Восстановление исходной проницаемости зависит от
скорости ферментативного разрушения цАМФ, эту функцию выполняет имеющаяся
внутри клетки фосфодиэстераза цАМФ.
Таким образом, активация V2—рецепторов вазопрессином сопровождается
образованием цАМФ и увеличением проницаемости для воды.
Выше речь шла о V1—рецепторах. Их физиологическое
значение состоит в модуляции, регуляции силы ответа клетки, они обеспечивают
осуществление своеобразной системы обратной связи. При регуляции водного обмена
в организме ведущую роль играет лишь один гормон — вазопрессин.
В регуляции ионного обмена обычно
природа использует два гормона, оказывающие противоположное физиологическое
действие, например кальцитонин, снижающий концентрацию кальция в крови,
и паратгормон, увеличивающий ее.
В случае вазопрессина можно описать уникальный
способ физиологической регуляции, когда один гормон с помощью рецепторов
двух разных типов стимулирует реакцию и модифицирует ее. Активация V1—рецепторов и образование описанных
выше вторичных мессенджеров способствуют снижению силы действия цАМФ.
Экспериментально можно активировать только аденилатциклазу и устранить
фосфоинозитидный ответ, связанный со стимуляцией V1—рецепторов. В
таком случае сила ответа на вазопрессин станет выше.
Эти данные позволяют представить
целостную картину регуляции водного обмена: от возбуждения осморецепторов и
секреции вазопрессина до конечных этапов внутриклеточных изменений,
сопровождающихся возрастанием проницаемости мембраны для воды. Поток воды при
увеличении ее реабсорбции растет в десятки раз.
Выше шла речь о процессах,
происходящих в базальной мембране, цитоплазме и апикальной мембране. Такие
большие физиологические изменения, сопровождающиеся возрастанием потока воды,
затрагивают и внешнюю поверхность клетки. После добавления вазопрессина наблюдается
экзоцитоз — выделение веществ со стороны апикальной мембраны на ее
внешнюю поверхность. Среди этих веществ находятся компоненты гликокаликса, а
также, вероятно, и ряд гидролитических ферментов.
А. Г. Гинецинский высказал предположение,
что на одном из этапов действия АДГ в процесс вовлекается гиалуронатгидролаза,
деполимеризующая гликозаминогликаны в межклеточном веществе почки. В пользу
такого предположения свидетельствуют данные, что введение в кровь антисыворотки
к почечной гиалуронатгидролазе уменьшает способность АДГ увеличивать
проницаемость для воды и ее реабсорбцию.
13.6.8. Механизм участия почек в регуляции
кислотно—основного равновесия
Почки играют важную роль в
поддержании постоянства концентрации ионов водорода в крови, экскретируя кислые
продукты обмена. Активная реакция мочи у человека и животных может очень резко
меняться в зависимости от кислотно—основного состояния в организме.
Концентрация ионов Н+ при крайних состояниях работы почек
различается почти в 1000 раз, при подкислении мочи рН в некоторых случаях
снижается до 4,5, при подщелачивании — достигает 8. Это способствует участию
почек в стабилизации рН плазмы крови на уровне 7,36. Механизм подкисления мочи
основан на секреции клетками канальцев ионов водорода (рис. 13.15).
В апикальной плазматической мембране
и цитоплазме клеток различных отделов нефрона находится фермент карбоангидраза,
катализирующая реакцию гидратации оксида углерода:
|
|
Секреция ионов Н+ создает
условия для реабсорбции вместе с НСОз— эквивалентного количества
ионов Na+. Наряду с Na/K ионообменным насосом и электрогенным натриевым насосом,
обусловливающим перенос натрия и хлора, реабсорбция Na+ и НСОз—
играет важную роль в натриевом балансе организма.
Фильтрующийся из плазмы крови
бикарбонат соединяется с ионами водорода, секретированными клеткой, и в
просвете канальца превращается в оксид углерода (см. рис. 13.15). Образование
ионов водорода для секреции происходит внутри клетки, где вследствие гидратации
СО2 возникшая угольная кислота диссоциирует на ионы Н+ и
НСО3—. В просвете канальца ионы водорода связываются не
только с бикарбонатом, но и с такими соединениями, как двузамещенный фосфат (Na2HPO4), и некоторыми другими, в
результате чего увеличивается экскреция титруемых кислот (ТА—) с
мочой. Это способствует выделению кислот и восстановлению резерва оснований в
плазме крови.
Наконец, секретируемые ионы водорода
могут связываться в просвете канальца с аммиаком, выделяющимся в клетке из
глутамина и аминокислот и диффундирующим через мембрану в просвет канальца, в
котором образуется ион аммония NН3 + H+ →NH4+.
Образование аммонийных солей нелетучих кислот способствует сбережению в
организме ионов Na+ и К+, которые реабсорбируются в
канальцах.
Таким образом, общая экскреция
кислот почкой (Uн + V) складывается из трех компонентов: количества
титруемых кислот (uтаv), количества выделенного аммония (UNН4+ V) и выводимого почкой бикарбоната (UНСО3— V):
UН+ V = UТаV+ Unh4+ V – UНСО3— V.
При питании мясом образуется больше
кислот и моча становится кислой, а при потреблении растительной пищи рН мочи
сдвигается в щелочную сторону. При интенсивной физической работе из мышц в
кровь поступают значительные количества молочной и фосфорной кислот. В этих
условиях почки увеличивают выделение кислых продуктов с мочой.
Кислотовыделительная функция почек
во многом зависит от состояния кислотно—основного равновесия в организме. Так,
при гиповентиляции легких
|
|
|
Рис. 13.15 Реакции,
обеспечивающие участие почки в регуляции кислотно—основного равновесия |
происходит задержка СО2 и
снижается рН крови — развивается дыхательный ацидоз, при гипервентиляции
уменьшается давление CO2 в крови и растет рН крови —
возникает состояние дыхательного алкалоза. Если в крови нарастает
содержание ацетоуксусной и бета—оксимасляной кислот, то падает концентрация
бикарбоната в крови, развивается состояние метаболического ацидоза. Рвота,
сопровождающаяся потерей соляной кислоты, приводит к повышению концентрации НСО3—
в крови и метаболическому алкалозу.
Легкие и почки участвуют в
нормализации кислотно—основного равновесия. При дыхательном ацидозе
увеличивается экскреция H+ и реабсорбция НСО3—.
Метаболический ацидоз компенсируется гипервентиляцией легких. В конечном счете
почки стабилизируют концентрацию НСО3— в плазме крови на
уровне 26—28 ммоль/л, а рН — на уровне 7,36.
13.6.9. Экскреторная функция почки
Почки играют ведущую роль в
выделении из крови нелетучих конечных продуктов обмена и чужеродных веществ,
попавших во внутреннюю среду организма. В процессе метаболизма белков и
нуклеиновых кислот образуются различные конечные продукты азотистого обмена,
выделяемые почкой. Обычно человек потребляет около 100 г белка в сутки. В этом
количестве содержится приблизительно 16
г азота. Основными азотсодержащими веществами мочи у человека являются
мочевина, мочевая кислота, креатинин, ион аммония.
Катаболизм пуриновых оснований в организме человека
завершается образованием мочевой кислоты. В клетках некоторых животных
имеется полный набор ферментов, обеспечивающих распад пуриновых оснований до С02
и NН3.
Мочевая кислота в почке человека фильтруется в клубочках, затем реабсорбируется
в канальцах, часть мочевой кислоты секретируется клетками в просвет нефрона.
Обычно у человека экскретируемая фракция мочевой кислоты довольно низка — 9,8%,
что указывает на реабсорбцию значительных ее количеств в канальцах.
Весь образующийся в течение 1 сут креатинин
выделяется почками с мочой. Его источником служит креатинфосфорная кислота, от
нее отщепляется фосфат, после чего в результате дегидратации креатина
образуется креатинин. Его суточная продукция и экскреция зависят не столько от
потребления мяса с пищей, сколько от мышечной массы тела. Креатинин, как и
мочевина, свободно фильтруется в почечных клубочках. Креатинин в основном
экскретируется почкой, мочевина частично реабсорбируется в канальцах.
В нормальных условиях даже физиологически ценные вещества
при их избытке в крови начинают экскретироваться почкой в больших количествах.
Это относится как к воде и неорганическим ионам, так и органическим веществам,
таким как глюкоза, аминокислоты. В небольших количествах в мочу поступают
некоторые производные продуктов гниения в кишечнике — индола, скатола, фенола,
которые обезвреживаются в печени, где образуются парные соединения с серной
кислотой. Это индоксилсерная, скатоксилсерная и другие кислоты.
С мочой выделяются различные биологически активные вещества
и продукты их превращения, по которым в известной степени можно судить о
функции некоторых желез внутренней секреции. В моче обнаружены производные
гормонов коры надпочечника, эстрогены, антидиуретический гормон, катехоламины,
различные витамины (аскорбиновая кислота, тиамин), ферменты (амилаза, липаза,
трансаминаза) и др. В условиях патологии в моче обнаруживаются вещества, обычно
в ней не выявляемые, — ацетон, жёлчные кислоты, белок и пр.
Помимо перечисленных существует еще очень много
разнообразных веществ, непрестанно удаляемых почкой из крови. Они могут
поступать в мочу и экскретироваться из
организма либо после фильтрации реабсорбироваться клетками канальцев,
подвергаться в них гидролизу или превращению, как, например, пептиды и
измененные белки, и всасываться в кровь. О том, какие вещества выводит или
разрушает почка, отчасти судят по составу крови после удаления почек. В плазме
крови накапливаются не только мочевина, креатинин, мочевая кислота, но и
гормоны (глюкагон, паратгормон, гастрин), ферменты (рибонуклеаза, ренин),
индолы, глюкуроновая кислота, алифатические амины и многие другие вещества.
Цвет мочи зависит от величины диуреза и экскреции пигментов, он
изменяется от светло—желтого до оранжевого. Эти пигменты образуются из
билирубина жёлчи в кишечнике, где билирубин превращается в уробилин и урохром,
которые частично всасываются в кишечнике и выделяются почкой. Часть пигментов
мочи представляет собой окисленные в почке продукты распада гемоглобина.
13.7. НЕРВНАЯ РЕГУЛЯЦИЯ ДЕЯТЕЛЬНОСТИ
ПОЧКИ
Почка — один из важнейших органов,
обеспечивающих гомеостаз, так как она служит исполнительным органом в цепи
различных рефлексов, регулирующих, постоянство состава и объема жидкостей
внутренней среды. Регуляция деятельности почки, адекватная информации о
состоянии внутренней среды, которая поступает в ЦНС, обеспечивается при участии
эфферентных нервных волокон или эндокринных желез. Гормоны играют важнейшую
роль в изменении процесса мочеобразования.
Работа почки, как и других органов, подчинена не только
безусловнорефлекторному контролю, но и регулируется корой больших полушарий
головного мозга; скорость мочеобразования может меняться условнорефлекторным
путем. В лаборатории Л. А. Орбели было показано, что прекращение
мочеотделения, наступающее при болевом раздражении, может быть воспроизведено
условнорефлекторным путем, в результате стимуляции секреции АДГ нейрогипофизом.
Условнорефлекторным путем может быть вызвано и увеличение диуреза: в
лаборатории К. М. Быкова было установлено, что многократное введение воды в
организм собаки в сочетании с условным раздражителем также приводило к образованию
условного рефлекса, при котором усиливалось мочеотделение.
В настоящее время показано, что при участии эфферентных
нервных волокон, подходящих к почке, регулируются не только ее гемодинамика и
работа юкстагломерулярного аппарата, но и процессы реабсорбции и секреции
неэлектролитов (глюкоза, ПАГ) и электролитов (натрий, фосфаты и др.) в
канальцах. Адренергические волокна стимулируют транспорт натрия,
холинергические волокна активируют реабсорбцию глюкозы и секрецию органических
кислот. Механизм изменения мочеообразования при участии адренергических нервов
связан с активацией аденилатциклазы и образованием цАМФ в клетках канальцев.
Чувствительная к катехоламинам аденилатциклаза содержится в базолатеральных
мембранах клеток дистального извитого канальца и начальных отделов
собирательных трубок.
Афферентные нервные волокна почки играют существенную роль в
качестве информационного звена системы реноренальных рефлексов.
13.8.
ИНКРЕТОРНАЯ ФУНКЦИЯ ПОЧКИ
В почке образуются и выделяются в
кровоток физиологически активные вещества, действующие на другие органы и
ткани, а также обладающие выраженным влиянием в самой почке. К веществам,
оказывающим системное и локальное действие, относятся ренин, эритропоэтин,
активная форма витамина D. В ткани почки выделяются также преимущественно локально
действующие вещества, влияющие в основном на ее работу, — простагландины
и брадикинины.
Наибольшее количество данных об
осуществлении инкреторной функции почки связано с юкстагломерулярным
аппаратом. Юкстагломерулярный аппарат расположен у входа в клубочек между
приносящей и выносящей артериолами клубочка и частью стенки дистального
канальца. В него входят гранулярные клетки афферентной артериолы, клетки
плотного пятна дистального канальца и специальные клетки, контактирующие с обеими
из перечисленных
выше групп клеток.
Более 90% гранул, содержащих ренин,
сосредоточено в клетках стенки афферентной артериолы. Ренин является
протеолитическим ферментом. Секретируемый в кровоток ренин отщепляет в плазме
от ангиотензиногена
ангиотензин I.
Под действием фермента от ангиотензина I, состоящего из 10
аминокислот, отщепляются две аминокислоты и образуется сильное сосудосуживающее
вещество — ангиотензин II. Ангиотензин II влияет на тонус сосудов, скорость
реабсорбции Na+ клетками канальцев, является важнейшим физиологическим стимулятором
секреции альдостерона клетками коры надпочечника. Ангиотензин II очень быстро
инактивируется в крови ангиотензиназами.
Описано много различных факторов, влияющих на скорость
секреции ренина. Кратко охарактеризуем лишь два из них. Одним из стимулов
является повышение концентрации NaCI в дистальном канальце. Это
способствует секреции ренина в юкстагломерулярном аппарате данного клубочка. В
нем снижается фильтрация и предотвращается возможность избыточной потери NaCI.
Удержание этой соли в организме равнозначно сохранению объема внеклеточной
жидкости и плазмы крови.
Другим важным стимулом служит раздражение рецепторов
растяжения, локализованных в стенке афферентной артериолы. Уменьшение ее
кровенаполнения активирует выделение ренина. Гомеостатическое значение обеих
реакций очевидно — вызванное секрецией ренина снижение клубочковой фильтрации
приведет к сохранению циркулирующего объема и предотвратит потерю почкой
избыточного количества солей натрия. Из этих данных становится понятной
стратегически важная анатомическая локализация юкстагломерулярного аппарата,
которая позволяет воспринимать изменения в составе канальцевой жидкости в том
же самом нефроне в процессе мочеобразования и одновременно участвовать в
регуляции клубочковой фильтрации и объема циркулирующей жидкости.
Таким образом, выделение ренина и образование ангиотензина
имеет исключительное значение для циркуляторного гомеостаза: происходит сужение
сосудов, приходит в соответствие с потребностями организма гемодинамика почки,
под влиянием альдостерона усиливается реабсорбция солей натрия, способствуя
сохранению объема внеклеточной жидкости в организме.
В последние годы были получены доказательства новой
гормонобразующей функции почки, связанной с регуляцией обмена кальция и
по своему биохимическому механизму напоминающей процессы, протекающие в коре
надпочечника. Почки извлекают из крови прогормон — 25—ОН—витамин D3, который образуется в печени,
накапливают его, в митохондриях осуществляют гидроксилирование и
превращение в 1,25—(ОН)2—витамин D3. Последний служит активным стероидным гормоном,
стимулирующим образование Са—связывающего белка в клетках кишечника, что
необходимо для всасывания Са2+. Этот же гормон способствует
высвобождению Са2+ из кости.
В почке образуется эритропоэтин, стимулирующий
образование эритроцитов в костном мозгу. Особенно этот процесс активируется при
гипоксии. В почке образуются кинины. В ней выделяется пептидаза —
калликреин, который отщепляет кинин от кининогена во фракции α2—глобулинов.
Почечные кинины (например, брадикинин) являются сильными вазодилататорами,
участвующими в регуляции почечного кровотока и выделения натрия.
В мозговом веществе почки синтезируются простагландины.
Под влиянием простагландина E2 увеличивается почечный кровоток и растет выделение Na+ без изменения клубочковой
фильтрации, по—видимому, вследствие угнетения реабсорбции его солей и воды в
проксимальном канальце. Простагландин Е2 уменьшает реакцию клеток
канальца на АДГ. Эти данные имеют важное значение, ибо они свидетельствуют о
возможности изменения реакции на гормон под влиянием образующихся в органе
физиологически активных веществ в частности простагландинов.
Почки играют определенную роль в регуляции состояния системы
свертывания крови. В них синтезируется активатор плазминогена — урокиназа. Фибринолитическая активность крови,
взятой в почечной вене, значительно выше чем в почечной артерии.
13.9. МЕТАБОЛИЧЕСКАЯ ФУНКЦИЯ ПОЧКИ
Участие почки в гомеостазе белков,
липидов и углеводов ранее недооценивали. Это участие не ограничено способностью
к реабсорбции данных соединений или экскреции их избытка.
В почке происходит образование и
разрушение различных пептидных гормонов, циркулирующих в крови, образование
глюкозы (глюконеогенез), превращение аминокислот, например глицина в серии,
необходимый для синтеза фосфатидилсерина, который участвует в образовании и
обмене плазматических мембран в различных органах.
Следует разграничить понятия метаболизм
почки и метаболическая функция почки. Метаболизм, обмен веществ в
почке, обеспечивает выполнение всех ее функций, метаболическая функция
почки связана с поддержанием в жидкостях внутренней среды стабильного уровня
ряда углеводов, белков и липидов.
Через фильтрующую мембрану клубочка
практически не проходят альбумины и глобулины, но свободно фильтруются пептиды.
Тем самым в канальцы непрестанно поступают гормоны, измененные белки. Их
расщепление имеет двоякое физиологическое значение — организм освобождается от
физиологически активных веществ, что улучшает точность регуляции, а в кровь
возвращаются аминокислоты, используемые для последующих синтезов. Имеющиеся
данные указывают на возможность извлечения некоторых белков и полипептидов
клетками нефрона из околоканальцевой жидкости и их последующего
разрушения.
Таким образом, почка играет важную
роль в расщеплении низкомолекулярных и измененных (в том числе
денатурированных) белков. Это объясняет значение почки в восстановлении фонда
аминокислот для клеток органов и тканей, в быстром устранении из крови
физиологически активных веществ и сохранении для организма их компонентов.
Почка не только потребляет глюкозу в процессе обмена, но и
обладает способностью к значительной ее продукции. В обычных условиях скорости
двух последних процессов равны. Использование глюкозы для выработки энергии в
почке составляет около 13% общего потребления кислорода почкой. Глюконеогенез
происходит в коре почки, а наибольшая активность гликолиза характерна
для мозгового вещества почки.
Почка обладает весьма активной системой образования глюкозы,
ее интенсивность на 1 г массы почки больше, чем в печени. При длительном
голодании в почках образуется половина общего количества глюкозы, поступающей в
кровь. Для этого используются органические кислоты, которые превращаются в
глюкозу, являющуюся нейтральным веществом, что способствует одновременно
регуляции рН крови. При алкалозе, напротив, снижен уровень глюконеогенеза из
кислых субстратов. Зависимость скорости и характера глюконеогенеза от величины
рН является особенностью углеводного обмена почки по сравнению с печенью.
Превращение различных субстратов в глюкозу, поступающую в
общий кровоток и доступную для утилизации в различных органах и тканях,
свидетельствует о том, что почке присуща важная функция, связанная с участием в
энергетическом балансе организма.
Почка оказалась основным органом окислительного катаболизма инозитола.
В ней миоинозитол окисляется в ксилулозу и затем через ряд стадий в глюкозу. В
ткани почки синтезируется фосфатидилинозитол, являющийся необходимым
компонентом плазматических мембран. Синтез глюкуроновой кислоты имеет большое
значение для образования гликозаминогликанов, содержание которых высоко в
межклеточной ткани внутреннего мозгового вещества почки и столь существенно для
процесса осмотического разведения и концентрирования мочи.
Участие в обмене липидов связано с тем, что свободные
жирные кислоты извлекаются почкой из крови и их окисление обеспечивает в
значительной степени работу почки. Так как свободные жирные кислоты связаны в
плазме с альбумином, то они не фильтруются, а их поступление в клетки нефрона
происходит со стороны межклеточной жидкости. Эти соединения окисляются в
большей степени в коре почки, чем в ее мозговом веществе. В почке образуются триацилглицерины.
Свободные жирные кислоты быстро включаются в фосфолипиды
почки, играющие важную роль в выполнении различных транспортных процессов. Роль
почки в липидном обмене состоит в том, что в ее ткани свободные жирные кислоты
включаются в состав триацилглицеринов и фосфолипидов и в виде этих соединений
поступают в циркуляцию.
Обсуждение механизмов работы экскреторных органов, особенно
почки, позволяет прийти к выводу, что главная функция выделительных органов
(почки, нефридии, солевые железы, жабры, потовые железы и др.) заключается в
поддержании постоянства физико—химических констант жидкостей
внутренней среды.
В ходе филогенеза и в процессе индивидуального развития
организмов ясно прослеживается тенденция удержания ведущих показателей состава
и объема крови во все более узких пределах, что расширяет адаптивные
возможности организмов в условиях меняющейся окружающей среды. В процессе
эволюции возрастает число функций, выполняемых почкой, наблюдается
интенсификация ее функций, возрастает дифференцировка образующих ее элементов,
усложняется структура системы регуляции ее функций. Это обеспечивает повышение
стабильности состава внутренней среды организма, что является абсолютно
необходимым условием для эффективной деятельности клеток различных органов и систем,
прежде всего мозга.
Образующаяся в почке или нефридии
моча у большинства животных накапливается в мочевом пузыре и затем
удаляется из организма. Лишь у некоторых видов животных (ряд костистых рыб,
акулы, скаты птицы и др.) мочевой пузырь отсутствует и моча из мочеточников
поступает в клоаку. У человека моча из выводных протоков поступает в почечную
лоханку Сокращение мускулатуры лоханки обеспечивает продвижение мочи в мочеточник,
по которому моча доставляется в мочевой пузырь. По мере увеличения количества
поступающей мочи пузырь растягивается, напряжение стенок остается постоянным и
давление внутри не растет. Когда объем жидкости в полости мочевого пузыря
достигает критического значения, круто нарастает напряжение его гладкомышечных
стенок, возрастает давление в полости пузыря и происходит мочеиспускание. Этот
акт является произвольным контролируемым, что обеспечивает переход мочи по
мочеиспускательному каналу наружу.
Рассмотрим некоторые особенности
взаимодействия ряда факторов, обеспечивающих выделение мочи. Растяжение стенок
мочевого пузыря приводит к раздражению механорецепторов. Само по себе
увеличение давления внутри пузыря без растяжения его стенок не вызывает такого
эффекта. Важное значение имеет скорость наполнения мочевого пузыря, в случае поступления в него жидкости
импульсация в афферентных волокнах тазового нерва резко возрастает. Опорожнение
мочевого пузыря сопровождается уменьшением напряжения его стенки и снижением
импульсации.
Регуляция процесса мочеиспускания
осуществляется в нервных центрах различного уровня. Импульсы от
механорецепторов мочевого пузыря поступают по афферентным нервам в крестцовые
отделы спинного мозга, где располагается рефлекторный центр мочеиспускания. Он
находится под контролем вышележащих отделов головного мозга — тормозные влияния
исходят из коры
головного мозга и среднего мозга,
возбуждающие — из моста и заднего гипоталамуса.
Корковые влияния, обеспечивающие
импульс к произвольному акту мочеиспускания, вызывают сокращение мышцы,
выталкивающей мочу (детрузора), возрастает давление внутри мочевого пузыря.
Происходит открытие шейки мочевого пузыря, расширение и укорочение задней части
мочеиспускательного канала (уретры), расслабляется образованный
поперечнополосатыми мышцами сфинктер. В результате сокращения мышц пузыря
давление в нем нарастает, а в уретре падает, что вызывает переход в фазу
опорожнения мочевого пузыря и удаление мочи наружу. Когда пузырь опустошается,
моча более не раздражает заднюю часть уретры, детрузор вновь расслабляется,
закрывается замыкательный аппарат и сокращается сфинктер.
ЗАКЛЮЧИТЕЛЬНЫЕ ЗАМЕЧАНИЯ
В эволюции живых организмов
отчетливо видна тенденция к развитию физиологических механизмов стабилизации
внутренней среды, что обеспечивало независимость от условий внешней среды. Гомеостаз,
т. е. способность организма сохранять динамическое постоянство состава и
свойств, достигается системой физиологических регуляций. Создание оптимальных
условий для работы клеток у высших многоклеточных организмов обеспечивается
высокой степенью постоянства условий во внутренней среде — на неизменном уровне
поддерживается объем крови, концентрация в ней неорганических и органических
веществ, рН, осмоляльности — суммарная концентрация всех растворенных веществ.
Последний показатель особенно важен для стабилизации объема клетки, ибо
уменьшение или увеличение осмоляльности крови тотчас приводит к набуханию или
сморщиванию клеток, что нарушает их работоспособность.
Поддержание постоянства объема и
состава жидкостей внутренней среды осуществляется под интегрирующим влиянием
ЦНС при участии многих органов — почек, кожи, желудочно—кишечного тракта,
тканевых депо. Специализированные тканевые барьеры обеспечивают высокую
степень стабильности концентрации ионов в жидкостях отдельных органов и систем:
спинномозговой, внутриглазной эндолимфе внутреннего уха и др. Гомеостаз
жидкостей внутренней среды имеет особое значение, поэтому в процессе эволюции
выработался ряд дублирующих механизмов обеспечения функций, их контроля,
регуляции.
Выделение веществ почкой находится
под нервным и гормональным контролем. Баланс кальция регулируется
по крайней мере тремя гормонами: кальцитонином, паратгормоном, активными
формами витамина D3. В организме имеется способность изменять реакцию клеток на уже
поступивший в кровь гормон. Так, вазопрессин не только увеличивает
проницаемость для воды, но и активирует секрецию простагландинов, снижающих
чувствительность рецепторов клеток к этому .же гормону.
Следовательно, многообразие форм
регуляции и участие клеток различных органов и систем обеспечивают способность
к исключительно высокой степени постоянства во внутренней среде организма в
условиях непрерывно меняющейся внешней среды.
Берхин Е. Б. Фармакология почек и ее физиологические основы. М., 1979.
Вандер А. Физиология почек. СПб., 2000.
Гинецинский А. Г. Физиологические механизмы водно—солевого равновесия. М.;
Л., 1964.
Глезер Г. А. Диуретики: Руководство для врачей. М., 1993.
Длоуга Г. Кршечек И., Наточин Ю. В. Онтогенез почки. Л., 1981.
Москалев Ю. И. Минеральный обмен. М., 1985.
Наточин Ю. В. Основы физиологии почки. Л., 1982.
Наточин Ю. В. Почка. Справочник врача. СПб., 1997.
Наточин Ю. В., Немцов В. И., Эмануэль В. Л. Биохимия крови и диагностика. СПб.,
1993.
Почечная эндокринология / Под ред. М. Дж. Данн. М., 1987.
Сравнительная физиология животных / Под ред. Л. Проссера. Т. 1. М.,
1977.
Физиология водно—солевого обмена и почки / Под ред. Ю. В. Наточина.
СПб., 1993.
Фролов Б. А. Физиология и патология кислотно—основного состояния. М.,
1998.
Шейман Дж. Патофизиология почки. М.; СПб., 1999.
Шюк О. Функциональное исследование почек. Прага, 1975.
Шмидт—Ниельсен К. Физиология животных. Приспособление
и среда. В 2 кн. М., 1982. Кн. 2.